
2024-09-23

文章題目:ARID1A safeguards the canalization of the cell fate decision during osteoclastogenesis(IF=14.7) 上海交通大學醫(yī)學院附屬上海市第九人民醫(yī)院口腔修復科在《Nature Communications》上發(fā)表了在破骨細胞發(fā)生過程中,ARID1A保護細胞命運決定的通道化的研究成果。本研究中轉(zhuǎn)錄組檢測及部分數(shù)據(jù)分析工作由上海派森諾生物科技股份有限公司完成。
1、研究背景 染色質(zhì)重塑子ARID1A通過調(diào)節(jié)核小體定位和染色質(zhì)可及性來調(diào)節(jié)基因轉(zhuǎn)錄。而在細胞命運通路中,ARID1A介導的階段和譜系限制基因調(diào)控仍未得到解決。
2、研究方法 研究材料 LysM-Cre小鼠、Arid1a-flox小鼠、Brd9-flox小鼠、WT C57BL/6J小鼠和tdTomato小鼠 技術(shù)手段 單細胞轉(zhuǎn)錄組測序(scRNA-seq)、轉(zhuǎn)錄組測序(RNA-seq)、共免疫沉淀(co-IP)、chip-seq、Western blot、qPCR
3、研究路線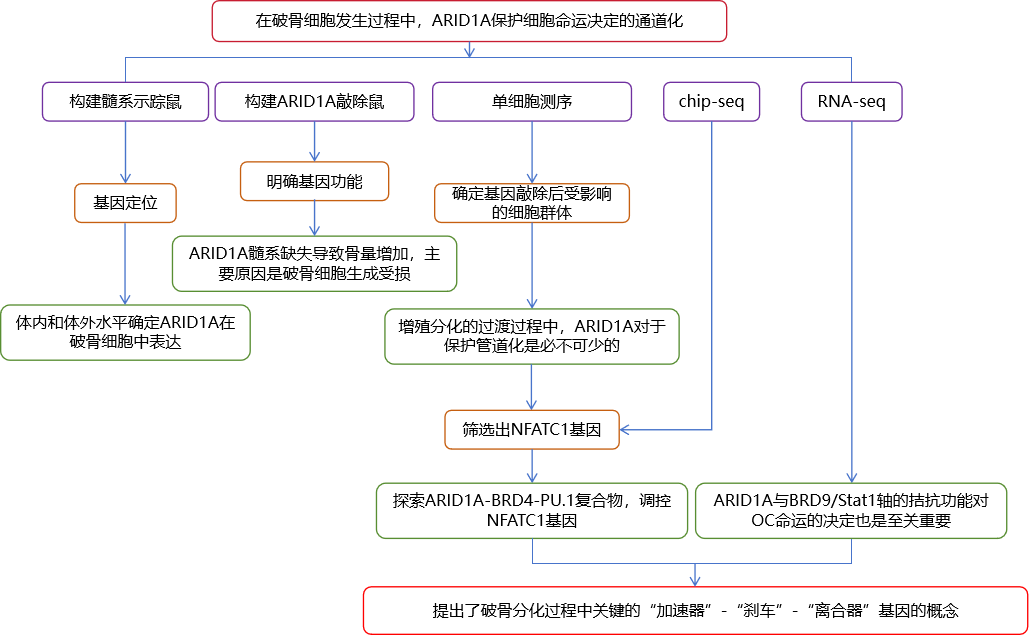
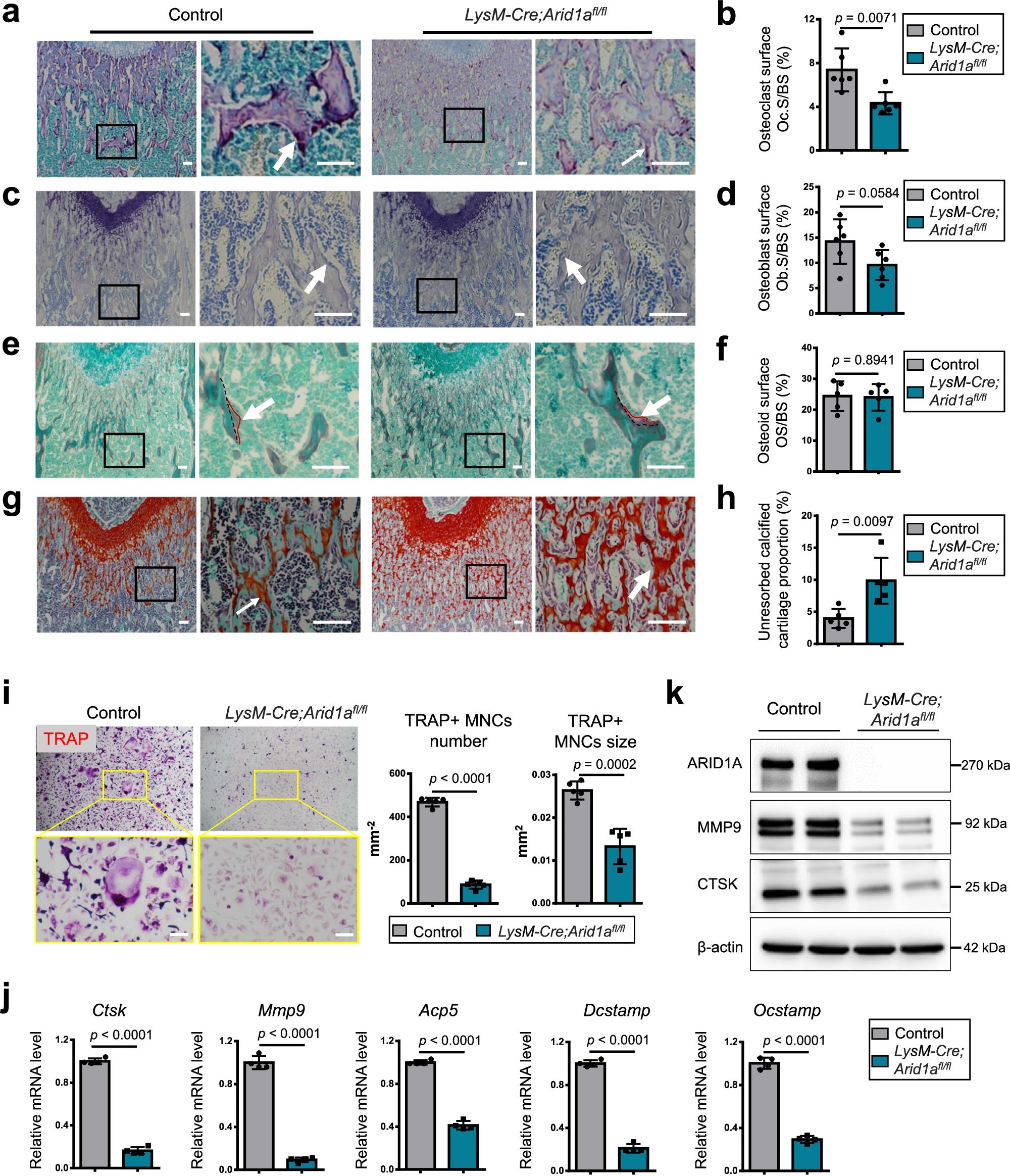
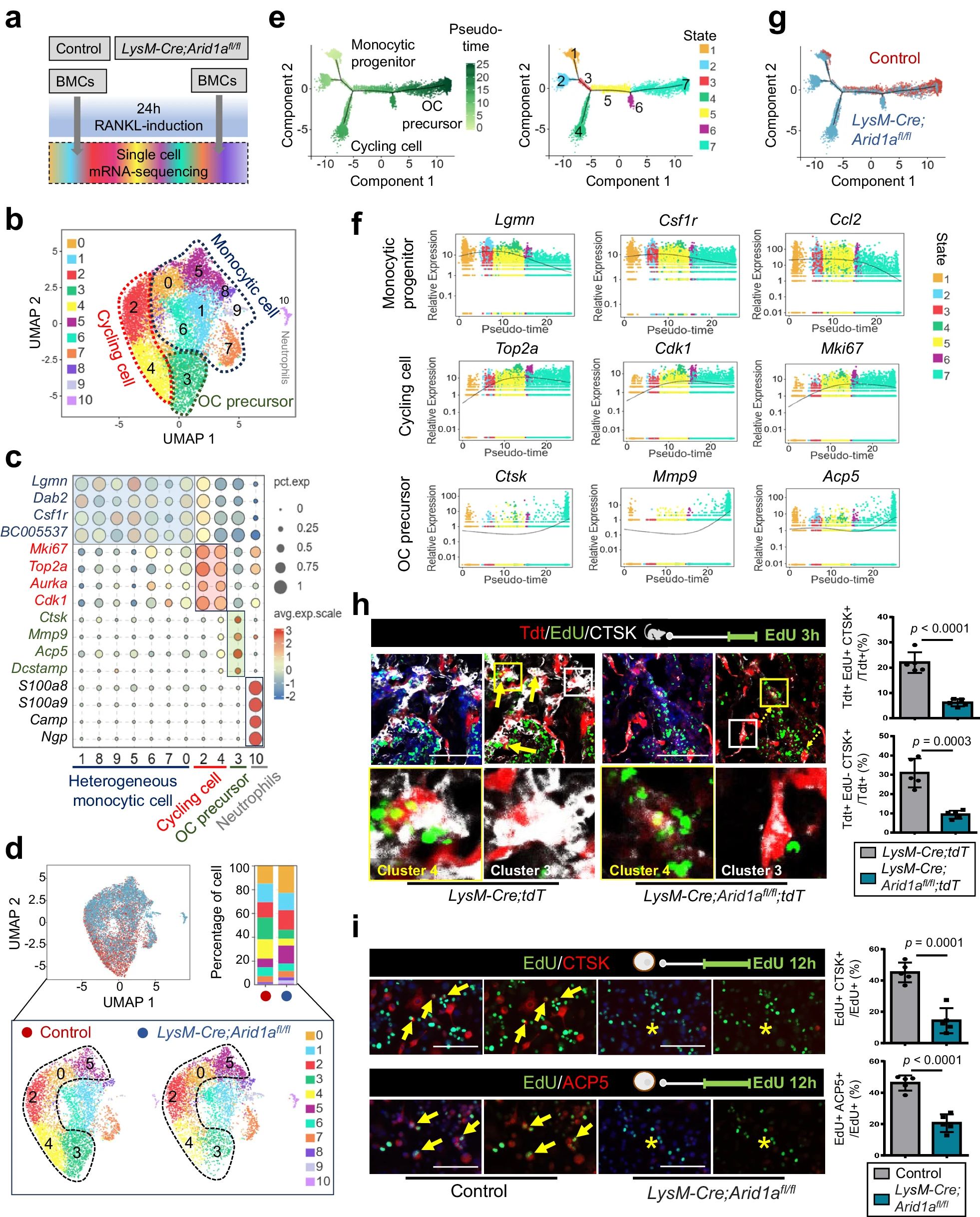
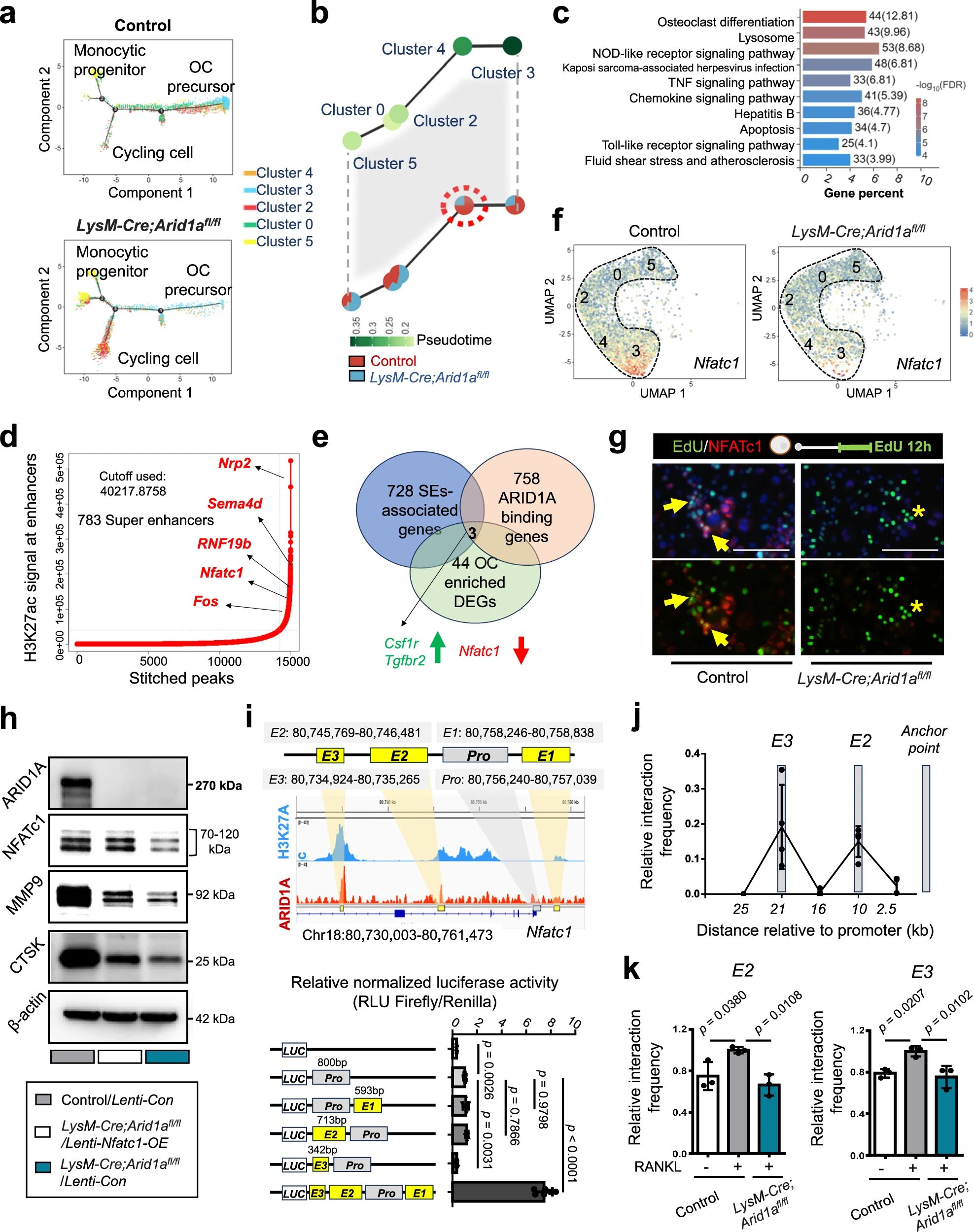
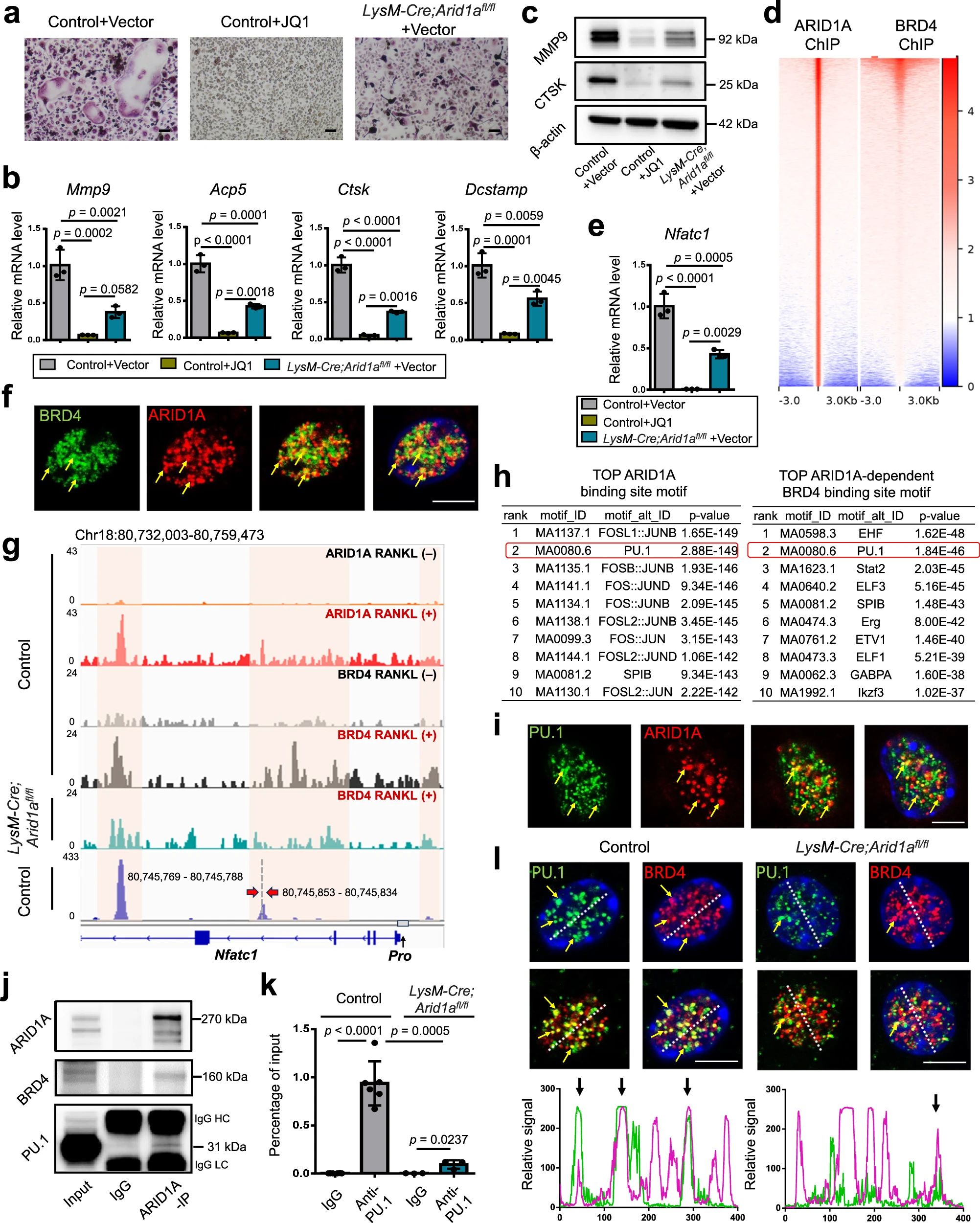
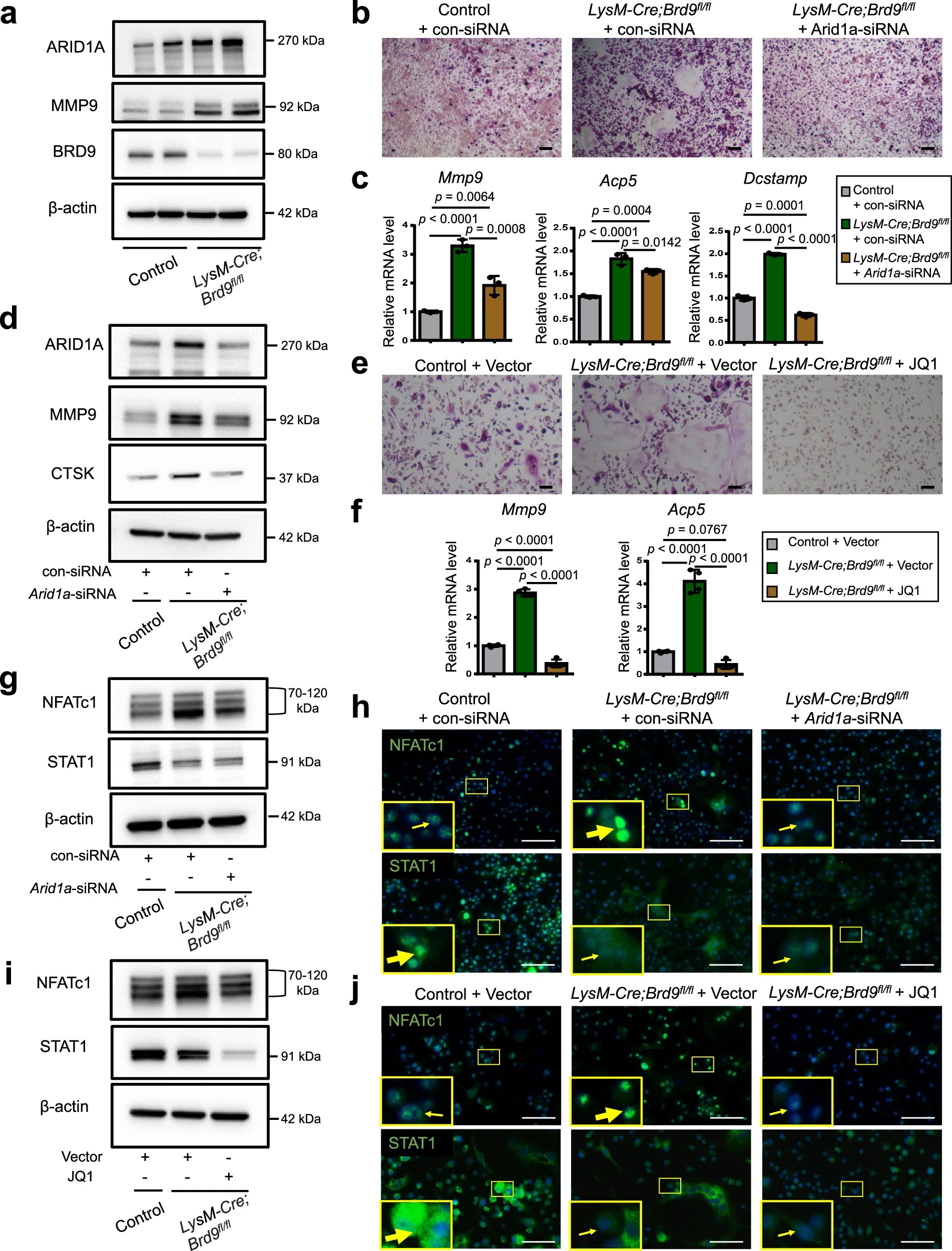
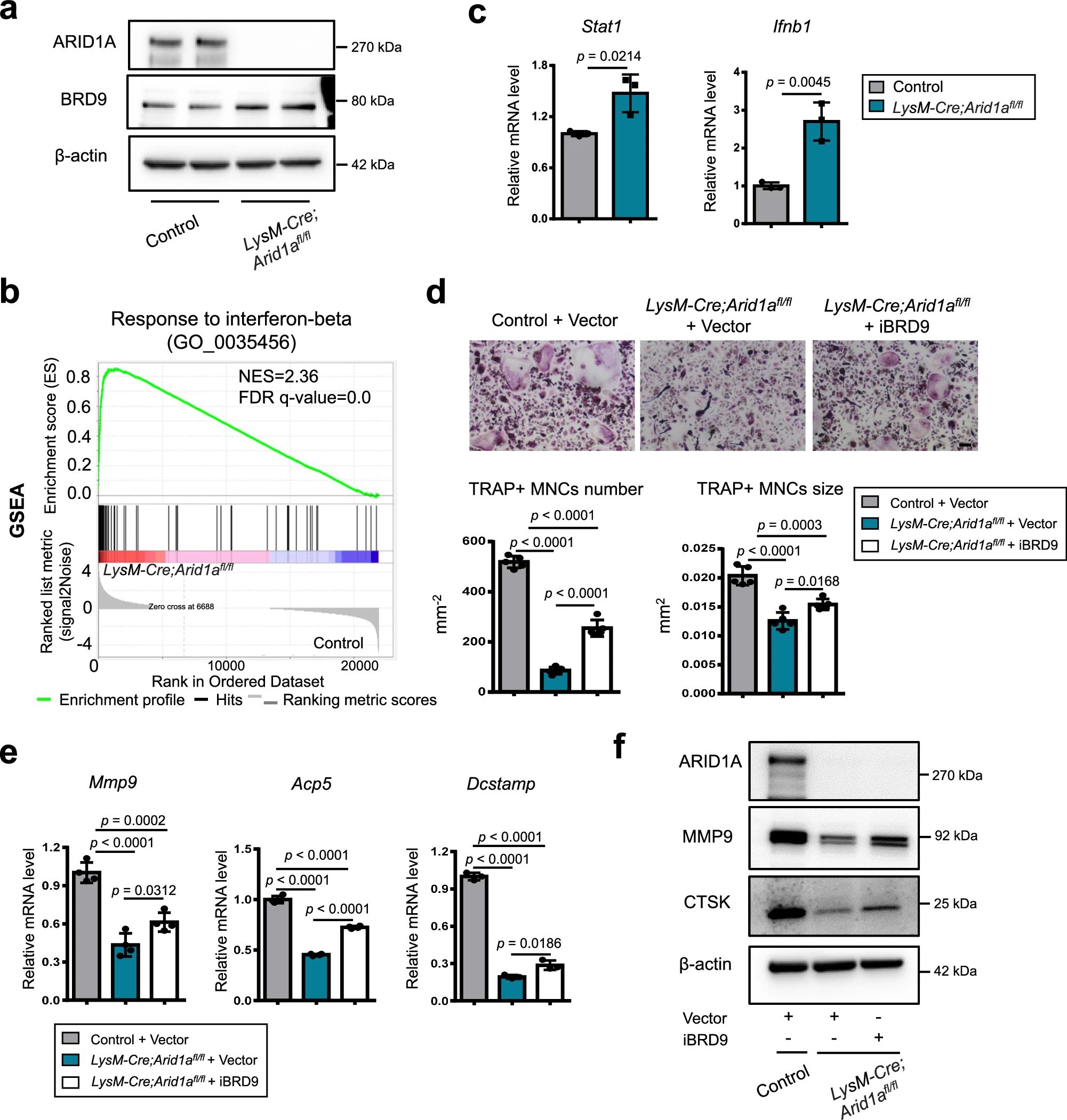
4、研究結(jié)果 1、Arid1a的缺失導致骨量過多,破骨細胞生成受損 構(gòu)建示蹤小鼠(LysM-Cre;tdT小鼠),結(jié)合CTSK(破骨標記物)和ARID1A熒光染色,發(fā)現(xiàn)ARID1A在4周齡小鼠股骨遠端骨小梁表面LysM+髓系破骨細胞中表達。體外誘導破骨細胞分化,進行TRAP和ARID1A的共染,發(fā)現(xiàn)ARID1A在體外TRAP+多核OC中表達,且經(jīng)RANKL處理后,ARID1A在mRNA和蛋白水平上的表達隨破骨誘導逐漸上調(diào)。 構(gòu)建ARID1A髓系敲除鼠(LysM-Cre;Arida1fl/fl)觀察表型:與對照雄性小鼠相比,3月齡雄性敲除鼠表現(xiàn)出骨小梁增加,骨體積/組織體積比(BV/TV)增加,骨礦物質(zhì)密度(BMD)增加,骨小梁數(shù)量增加,骨小梁厚度增加,骨小梁間距減少,孔隙率(Po)減少。HE染色和Von Kossa染色顯示,與3周齡和6周齡的同窩對照小鼠相比,Arid1a缺失小鼠骨量增加,礦化增加。(圖1) 圖1 髓系中Arid1a的缺失導致骨量過多 進一步分析3周齡成骨、破骨功能改變情況。TRAP染色顯示敲除鼠破骨細胞定量減少;甲苯安藍染色顯示成骨細胞定量減少;GRB染色顯示類骨質(zhì)定量相似;MASSON染色顯示敲除鼠股骨遠端生長板下存在大量未吸收的鈣化軟骨;骨髓單核細胞體外破骨誘導TRAP染色顯示敲除鼠TRAP陽性破骨細胞數(shù)量減少,體積變小;血清骨吸收(TRAP/CTX-I)和骨形成標志物(OCN/PINP),破骨指標蛋白qPCR,WB(MMP9,CTSK)顯示,敲除鼠骨吸收被抑制,骨形成能力無顯著變化。結(jié)果表明ARID1A敲除鼠骨量增加,破骨抑制。ARID1A對于正常的破骨分化至關(guān)重要。(圖2) 圖2 骨髓譜系中Arid1a的缺失導致OC譜系承諾受損 2、在增殖-分化轉(zhuǎn)換過程中,ARID1A轉(zhuǎn)錄保護OC命運通路 為了分析ARID1A對于破骨分化作用的內(nèi)在機制,對ARID1A缺失的骨髓細胞進行24小時的破骨誘導后做單細胞轉(zhuǎn)錄組測序(scRNA-Seq)。對照組5813個細胞,敲除組5305個細胞,聚類分析出11個聚類。其中簇3具有高表達的破骨相關(guān)基因,說明簇3是破骨細胞前體。其余(簇1,8,9,5,6,7,0)主要是單核細胞,簇2,4主要是增殖群體,簇10為中性粒細胞標記。比較各個聚類細胞簇比例,發(fā)現(xiàn)簇5、0和2的比例增加,而簇4和3的比例減少,說明ARID1A的缺失缺失影響了破骨細胞的分化。隨后進行偽時間分析,單核細胞祖細胞通過逐步途徑分化為OC前體細胞,單核祖細胞標記物Lgmn、Csf1r和Ccl2表達水平逐漸下調(diào),破骨基因Ctsk、Mmp9和Acp5表達逐漸增高,增殖標記基因的表達水平在中期達到峰值。對比敲除組和對照組的偽時間分析,發(fā)現(xiàn)ARID1A缺失后,單核細胞從增殖到分化的過程受到阻礙。體內(nèi)體外EDU示蹤標記細胞實驗顯示ARID1A缺失組,EUD陽性的CTSK+或者TRAP+細胞很少。結(jié)果表明在增殖分化的過渡過程中,ARID1A對于保護管道化是必不可少的,而在破骨細胞發(fā)生過程中,ARID1A的缺失會導致細胞命運承諾的缺陷。(圖3) 圖3 在增殖-分化轉(zhuǎn)換過程中,ARID1A轉(zhuǎn)錄保護OC命運通路 3、ARID1A在增殖-分化轉(zhuǎn)變過程中激活OC主TF Nfatc1的SE轉(zhuǎn)錄 為了進一步研究ARID1A介導的轉(zhuǎn)錄調(diào)控機制,重點研究了ARID1A缺失后分化軌跡中轉(zhuǎn)錄譜的變化。KEGG富集分析顯示,溶酶體、趨化因子信號通路和代謝途徑在簇5和簇0中高度富集,細胞周期和DNA復制在簇2中富集,核糖體相關(guān)途徑在簇3中高度富集,DNA復制和核糖體相關(guān)途徑在簇4中都富集。偽時間分析和基于分區(qū)的圖抽象(PAGA)均顯示,增殖-分化切換的關(guān)鍵細胞群簇4是Arid1a缺失后的主動缺陷細胞簇。然后分析了Arid1a缺失后簇4轉(zhuǎn)錄譜的變化。Arid1a缺失后,有1266個上調(diào)基因和503個下調(diào)基因,如預期的那樣高度富集于OC分化。 為了了解與ARID1A相關(guān)的轉(zhuǎn)錄增強子,對RANKL誘導的破骨細胞進行了ChIP-seq測序,從而獲得ARID1A和超級增強子SEs相關(guān)組蛋白修飾標記H3K27Ac的全基因組結(jié)合譜。確定了15039個增強子區(qū)域,其中783個SE區(qū)域在大小和H3K27Ac水平上與典型增強子不同。將所有轉(zhuǎn)錄活性基因(TSSs)分配到50 kb窗口內(nèi)的SEs上,鑒定出728個與SEs相關(guān)的基因,并提出NFATc1可能是調(diào)節(jié)破骨細胞終端分化的主開關(guān)。 單細胞測序內(nèi)結(jié)果發(fā)現(xiàn)Nfatc1的表達在分化過程中上調(diào),而在Arid1a缺失后的第4簇中沒有上調(diào),這表明它可能是Arid1a在OC命運決定過程中的核心下游靶點。對EdU標記的增殖細胞進行了12小時的追蹤,發(fā)現(xiàn)對照組中可以檢測到NFATc1+細胞,而失去Arid1a后則很少。通過使用慢病毒載體在敲除小鼠的BMCs中組成表達NFATc1。組成性表達的Nfatc1部分挽救了ARID1A缺失后的缺陷OC分化,增加了MMP9、CTSK和ACP5的表達。表明ARID1A和超級增強子相互作用,調(diào)控Nfatc1基因功能,影響破骨細胞分化。(圖4) 圖4 ARID1A在增殖分化轉(zhuǎn)換過程中激活Nfatc1的SE轉(zhuǎn)錄 4、ARID1A通過在SE位點與共激活劑BRD4和指定譜系的TF構(gòu)建凝聚體來激活Nfatc1 BRD4作為增強子的表觀基因組解讀器,與介質(zhì)相互作用,并通過SE(超級增強子)重編程和TF(轉(zhuǎn)錄因子)重連接活動參與轉(zhuǎn)錄延伸的控制。 引入BRD4后,首先進行BRD4抑制實驗,發(fā)現(xiàn)BRD4受JQ1抑制與ARID1A缺失之間的OC分化缺陷表型相似,TRAP+多核OC數(shù)量和大小均減少,Mmp9、Ctsk、Acp5和Dcstamp的表達均受到抑制。為了進一步研究ARID1A和BRD4在破骨細胞形成過程中的調(diào)控機制的相似性,我們比較了ARID1A和BRD4 (RANKL誘導前后)的結(jié)合譜。結(jié)果顯示OC分化過程只富集在ARID1A和BRD4的共有基因上,提示它們在破骨細胞發(fā)生過程中可能具有協(xié)同作用。考慮到ARID1A通過SE活性在OC細胞命運決定過程中不可或缺的功能,以及JQ1抑制BRD4和RANKL誘導后ARID1A缺失導致Nfatc1轉(zhuǎn)錄抑制,推測BRD4可能是激活Nfatc1 SE從而OC分化過程中的關(guān)鍵共激活因子。雙免疫熒光染色也驗證了BRD4在ARID1A細胞核中的共定位在破骨細胞發(fā)生中的作用。盡管BRD4的表達在mRNA和蛋白質(zhì)水平上都不受影響,但在Arid1a缺失后,BRD4在Nfatc1 SE區(qū)域的結(jié)合受到損害,Arid1a與BRD4在Nfatc1 SE區(qū)域的共定位依賴于RANK信號傳導。表明BRD4與Nfatc1 SE位點的ARID1A協(xié)同保護破骨細胞形成過程中的管道化,ARID1A的缺失導致BRD4在Nfatc1位點的激活功能缺陷。 為了確定在Nfatc1的SE位點與ARID1A合作以保護破骨細胞形成過程中的管道化的關(guān)鍵譜系指定轉(zhuǎn)錄因子,我們對ARID1A和BRD4結(jié)合譜進行了基序分析。ChIP-Seq數(shù)據(jù)顯示ARID1A有828個峰(p < 0.001), ARID1A依賴性BRD4結(jié)合有1298個峰(p < 0.001)。Ets家族TF PU.1在ARID1A結(jié)合位點的頂部富集TF基序中,以及在ARID1A耗盡后丟失的ARID1A依賴性BRD4結(jié)合位點中。PU.1是造血過程中一種指定譜系的TF,它正向調(diào)節(jié)許多共定位的PU.1- brd4點,提示為ARID1A-BRD4-PU。除PU.1外,NFKB1、AP-1和NFATc1基序也在NFATc1 SE區(qū)富集,表明其也可能參與ARID1A/BRD4/PU。(圖5) 圖5 ARID1A通過在SE位點與共激活劑BRD4/指定譜系的TF PU.1構(gòu)建凝聚體激活Nfatc1 5、ARID1A-cBAF和BRD9-ncBAF復合物在OC命運通路中的拮抗劑 近期研究表明,BRD9-ncBAF復合物通過STAT1/IFN-β信號激活負向調(diào)節(jié)OC分化,這與本研究中證實的ARID1A的功能相反。我們發(fā)現(xiàn)BRD9缺失BMC細胞中,ARID1A表達增強,破骨分化指標MMP9增強。使用siRNA敲低ARID1A或者JQ1抑制BRD4的活性,可以逆轉(zhuǎn)BRD9缺失造成的破骨分化過度。表明ARID1A-BRD4復合物軸參與了BRD9缺失造成的破骨增強。雖然BRD9缺失后過度激活的NFATc1被挽救,但在LysM-Cre的BMCs中,無論是siRNA敲低ARID1A還是JQ1抑制BRD4,STAT1的表達仍然處于低水平,表明挽救機制不依賴于STAT1。此外ARID1A缺失導致BRD9蛋白水平升高。(圖6) 圖6 ARID1A/BRD4/PU活性增強。1/NFATc1軸有助于Brd9缺失后過度激活的OC譜系測定 GSEA分析表明,與對照組相比,在RANKL誘導后,LysM-Cre;Arid1afl/fl小鼠BMCs中IFN-β信號富集。qPCR驗證表明ARID1A缺失后,破骨細胞誘導的BMCs中Stat1和Ifnb1表達增加。表明BRD9/STAT1/IFN-β信號軸參與ARID1A缺失導致的破骨細胞形成受損。在破骨細胞形成過程中使用BRD9抑制劑治療ARID1A缺失的BMCs。發(fā)現(xiàn)BRD9抑制部分挽救了Arid1a缺失后OC分化缺陷,增加了TRAP+多核OC的數(shù)量和大小以及Mmp9、Acp5、Dcstamp和Ctsk的表達水平。(圖7) 圖7 BRD9/STAT1軸的過度活性導致Arid1a缺失后OC分化過程受損 進一步建立BRD9雜合敲除LysM-Cre;Arid1afl/fl小鼠體內(nèi)模型,驗證這一假設(shè)。與3月齡雌性小鼠相比,LysM-Cre;Arid1afl/fl組的骨質(zhì)增生表型和OC分化缺陷在LysM-Cre;Arid1afl/fl;BRD9fl/+組得到部分恢復,ARID1A缺失后STAT1異常上調(diào)得到緩解。 ARID1A缺失導致BRD9蛋白水平升高,而mRNA水平無明顯變化,提示ARID1A缺失后BRD9轉(zhuǎn)錄后水平調(diào)控可能發(fā)生了變化。使用UbiBrowser 2.0軟件預測了BRD9潛在的E3連接酶/DUBs。整合前15個預測的泛素連接酶/DUBs,并比較對照組和LysM-Cre;Arid1afl/fl小鼠BMCs中RNA-seq數(shù)據(jù)的差異表達分析。E3泛素蛋白連接酶 MDM2在ARID1A缺失后顯著下調(diào)。SP141抑制劑44降解MDM2可以增加BRD9蛋白水平,表明ARID1A缺失后MDM2的下調(diào)可能有助于BRD9蛋白水平的升高。 因此,除了通過在SE位點與共激活因子BRD4/譜系指定因子PU.1構(gòu)建凝聚體激活OC主TF Nfatc1外,ARID1A與BRD9/Stat1軸的拮抗功能對OC命運的決定也是至關(guān)重要的。在增殖-分化轉(zhuǎn)換過程中,ARID1A的缺失導致Nfatc1上調(diào)和Stat1下調(diào)失敗。綜上所述,在OC譜系的分化傳導過程中,ARID1A-cBAF和BRD9-ncBAF復合物的功能相互拮抗,控制和維護命運決定過程。(圖8) 圖8 在體內(nèi),Brd9雜合敲除部分修復了Arid1a缺失后的OC分化缺陷 在BRD4抑制劑JQ1治療后,在ARID1A缺失的BMCs中,STAT1的表達水平下降,這表明ARID1A缺失后BRD9- STAT1軸的增強依賴于BRD4。BRD4通過與ARID1A-cBAF復合物的相互作用激活破骨細胞的主要轉(zhuǎn)錄因子 Nfatc1,并通過與BRD9-ncBAF復合物的相互作用增強IFN-β信號轉(zhuǎn)導/Stat1活性。我們的發(fā)現(xiàn)表明ARID1A-“加速器”和BRD9-“剎車”的拮抗作用都依賴于BRD4, BRD4發(fā)揮“離合器”作用。(圖9) 圖9 在破骨細胞發(fā)生過程中,ARID1A和BRD9的拮抗功能都依賴于BRD4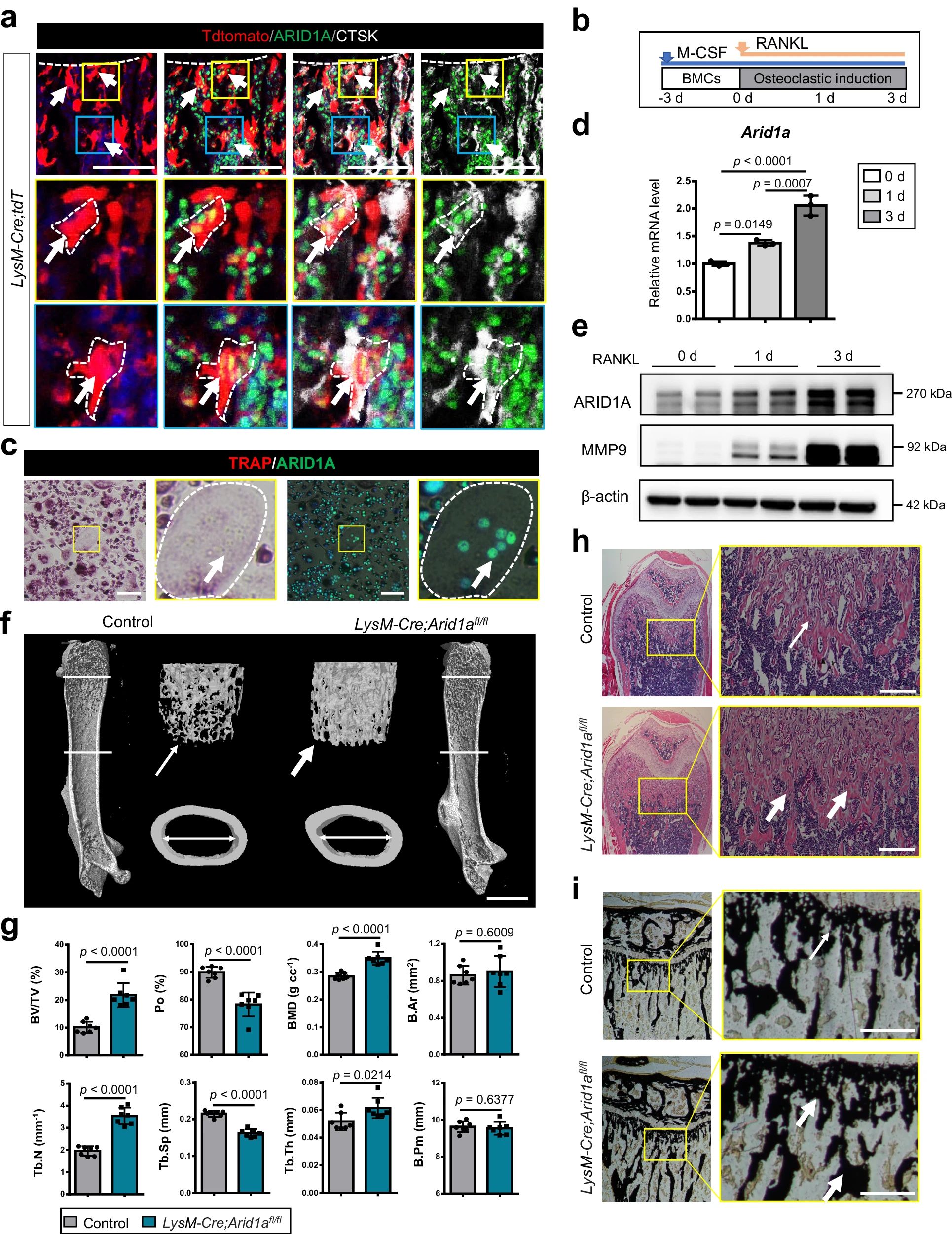
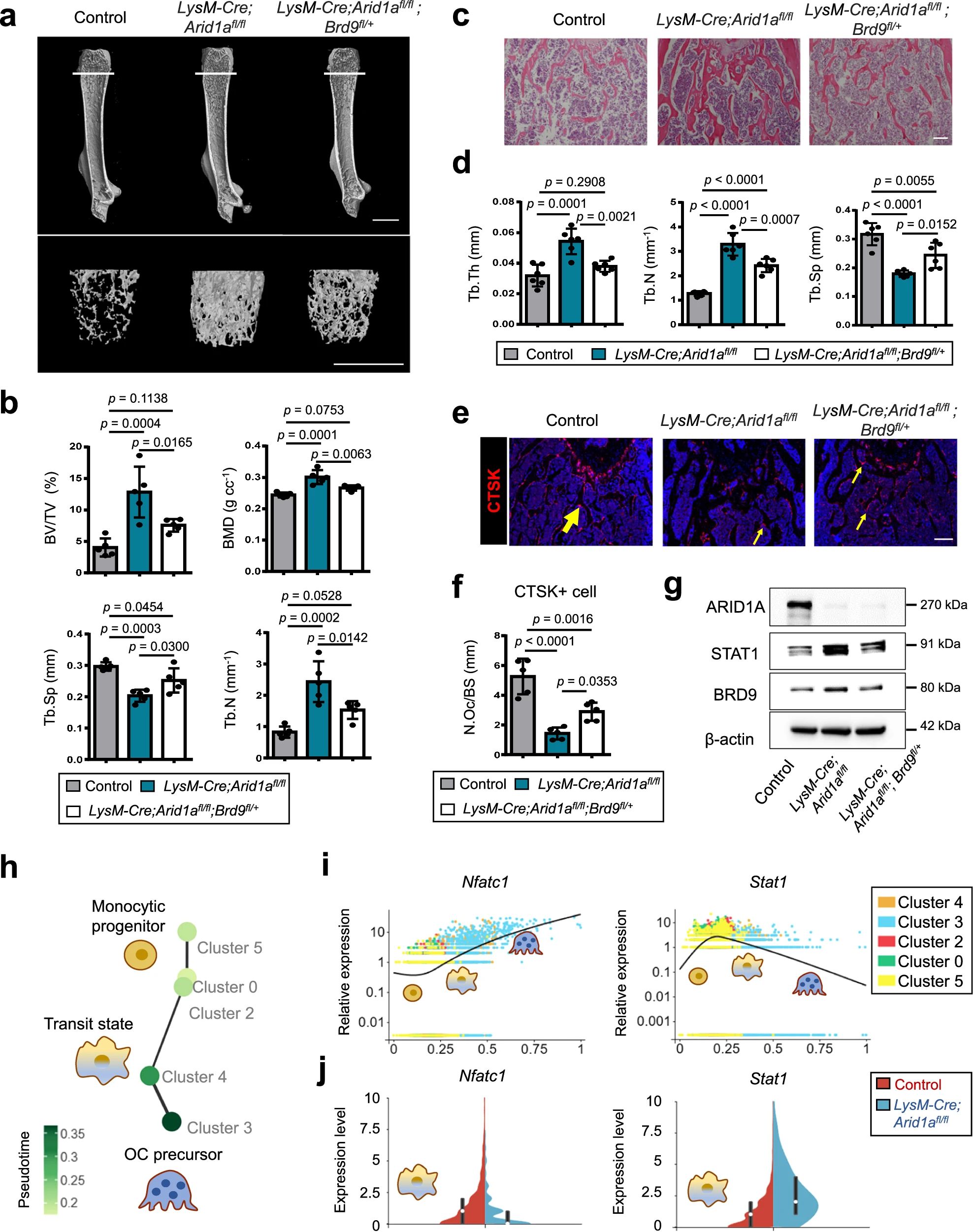
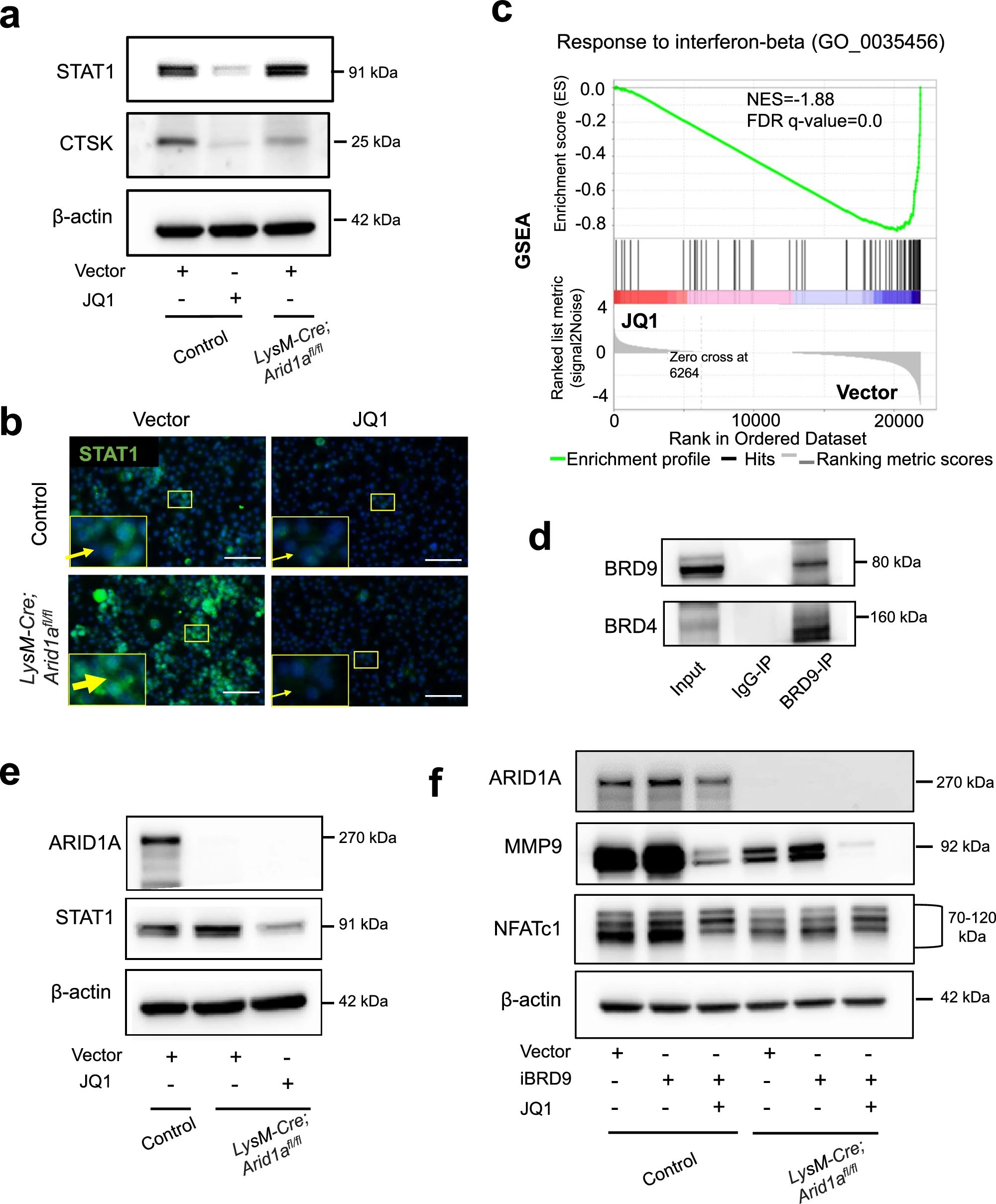
5、研究結(jié)論 1、骨髓祖細胞中Arid1a的缺乏會在增殖-分化轉(zhuǎn)換過程中損害OC譜系的分化,導致骨量過多。 2、ARID1A對于在主TF Nfatc1 SE區(qū)域與共激活子BRD4/指定譜系的TF PU.1形成轉(zhuǎn)錄裝置凝聚體是必不可少的,從而保護OC命運的渠化。 3、ARID1A-cBAF和BRD9-ncBAF復合物的功能相互拮抗,控制和維護命運決定過程。 4、ARID1A-“加速器”和BRD9-“剎車”的拮抗作用都依賴于協(xié)同激活劑BRD4-“離合器”在OC命運管化過程中。
原文索引: https://doi.org/10.1038/s41467-024-50225-z