
2023-10-17

《Small》
影響因子:13.3
文章題目:Covalently Grafted Biomimetic Matrix Reconstructs the Regenerative Microenvironment of the Porous Gradient Polycaprolactone Scaffold to Accelerate Bone Remodeling
四川大學生物材料國家工程研究中心在《Small》上發表了仿生基質重構3D打印梯度多孔支架再生微環境加速骨再生的研究成果。本研究中蛋白組檢測及部分數據分析工作由上海派森諾生物科技股份有限公司完成。
一、研究背景
天然骨組織的微觀結構中,堅實的無機成分(羥基磷灰石)主要負責支撐、保護和承重,而柔軟的有機成分(膠原纖維,多糖)在干細胞的增殖和遷移中起著重要作用。因此,有效地模擬天然骨軟硬結合的雜化的結構與功能,有助于調控干細胞命運來改善骨再生進程。3D打印技術可以用于組織工程支架結構的精確控制,特別是創建有序孔隙和用戶自定義結構,被廣泛應用于組織工程領域。然而,目前以PCL,PLA等為主的擠出式3D打印支架難以提供組織重塑過程中長期穩定的營養供給,同時其表面缺乏活性配體,這會導致無效的細胞粘附和下游細胞事件,難以模擬骨組織再生過程所需的生理微環境。因此尋找理想的骨再生性植入物仍然是臨床上一個持續的挑戰。
二、技術路線
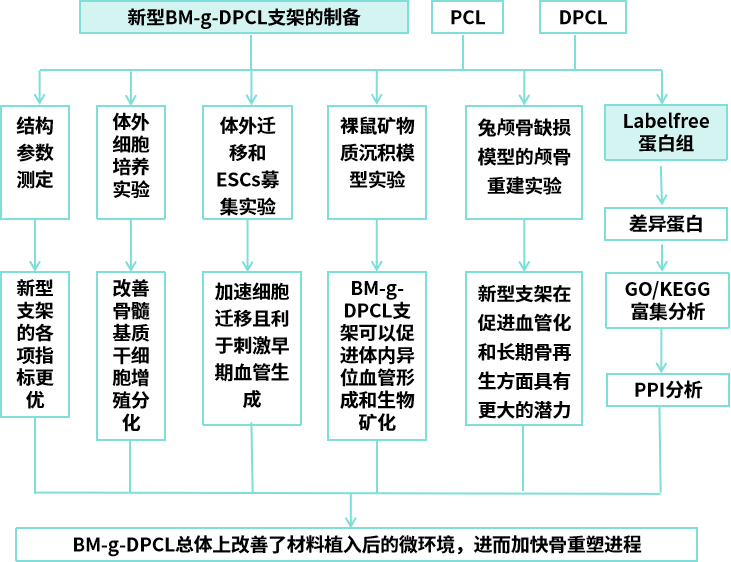
三、研究內容
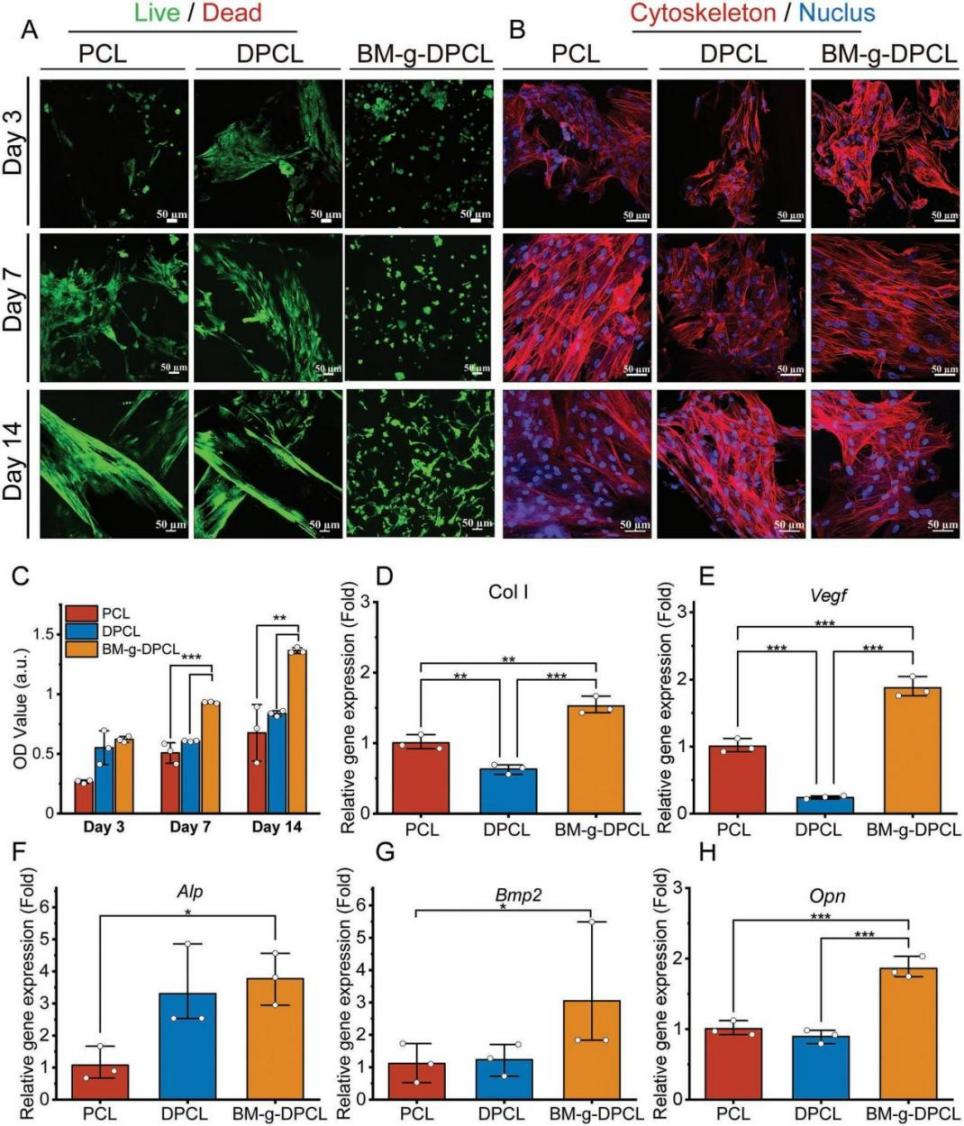
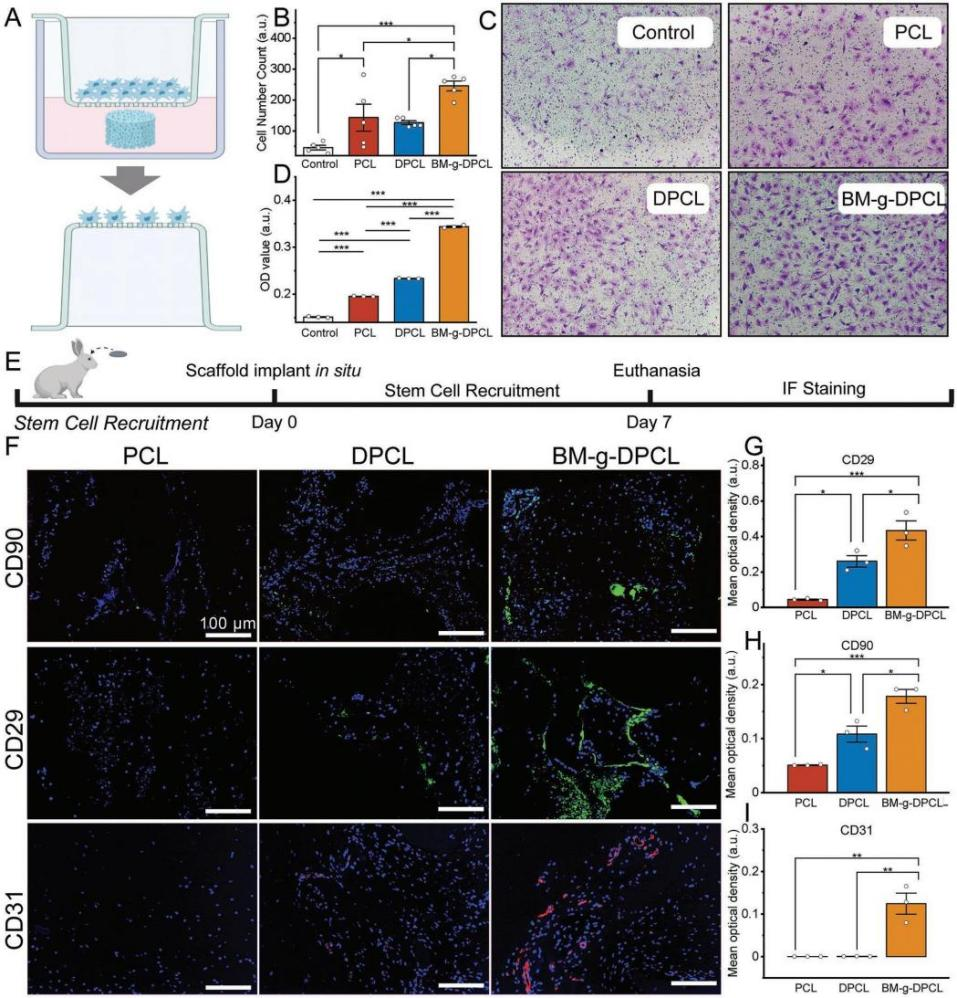
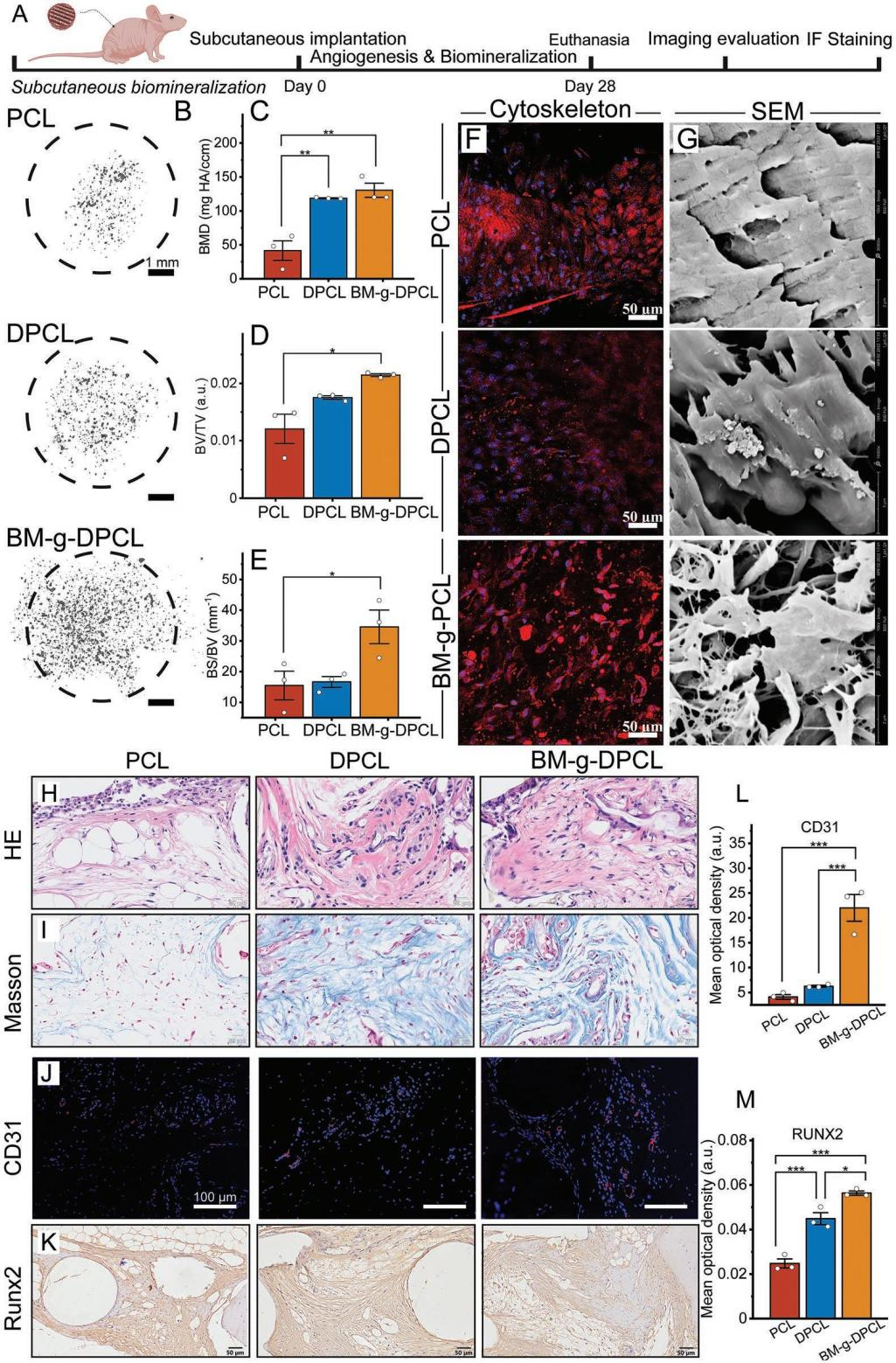
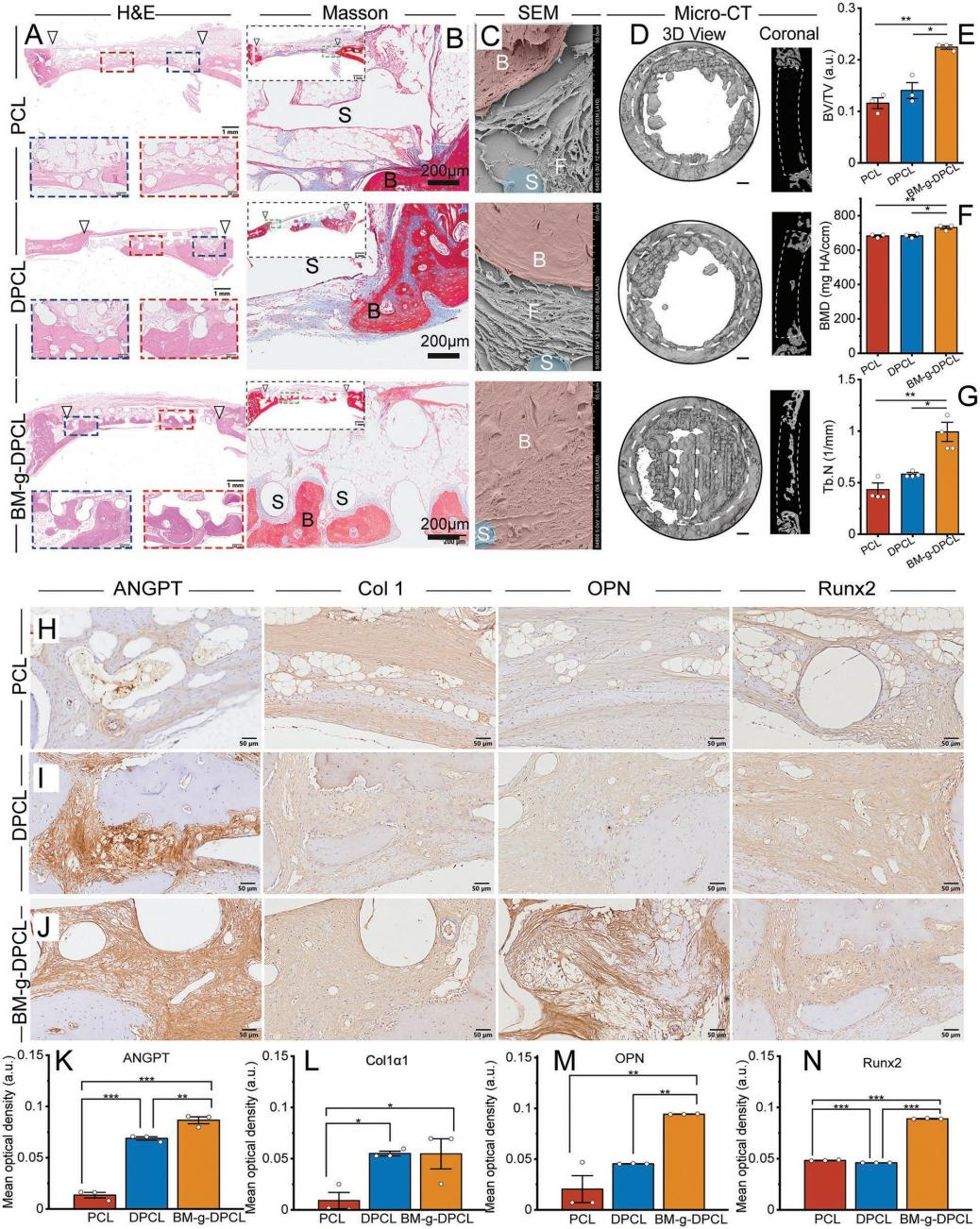
仿生基質修飾多巴胺涂層3DP梯度PCL支架的制備與表征 利用多巴胺介導的化學整合,將仿生胞外基質凝膠修飾在聚多巴胺涂層的3D打印PCL支架中,構建了軟-硬結合的活性骨修復體(BM-g-DPCL,圖1A)。采用原子力顯微鏡(AFM)和掃描電鏡(SEM)測量了表面形貌和粗糙度,發現DPCL表面粗糙度和表面高度均高于未涂層支架(圖1B-D),而PCL的水接觸角顯著高于DPCL(圖1E)。DPCL的親水性和粗糙的表面可能促進細胞和蛋白質的粘附。此外,DPCL纖維表面的PDA顆粒也顯著促進了鈣離子的螯合作用,并呈現出更強烈的綠色熒光,暗示潛在的礦物沉積能力(圖1F-I)。熱重分析曲線和差示掃描量熱分析結果(圖1J-L)顯示,BM-g-DPCL的最高變性溫度為402℃,相對而言,PCL為338℃,DPCL為345℃,說明兒茶酚誘導的多重鍵合反應增強了支架的熱穩定性。此外,生物活性基質約占BM-g-DPCL總重量的22%。低倍鏡下PCL和DPCL支架的顯微結構無明顯差異(圖1M-N)。然而,BM-g-DPCL支架的孔隙結構特征發生了明顯變化。膠原纖維和多糖透明質酸形成了大量的微孔(多為100-200μm,圖1O),這些微孔均勻分布在整個3d打印支架中,以高度仿生的軟硬結構構建骨修復體。 圖1BM-g-DPCL支架的制備與表征 支架對骨髓基質干細胞增殖分化的影響 共培養3、7和14天后,分別進行活/死染色和細胞骨架染色(圖2A-B),以評估細胞存活狀態和形態。根據激光掃描共聚焦顯微鏡(CLSM)的活/死染色圖像,支架中幾乎沒有可見的死細胞,表明支架與rBMSCs具有良好的生物相容性。由于只有支架的內部纖維能夠提供粘附位點,因此在14 d后,PCL和DPCL支架也可以看到明顯的定向生長以及內部纖維的生長,說明BM-gDPCL為細胞生長提供了優越的微環境。細胞骨架染色證實所有支架均支持細胞的擴散。 CCK-8檢測(圖2C)結果顯示,與PCL相比,在BM-g-DPCL中引入PDA涂層和生物活性水凝膠增強了rBMSCs的粘附和增殖。21天后,定量測量成骨(Ocn、Alp、Opn和Bmp2)和基質重塑相關(Col I和Vegf)基因的表達(圖2D-H)。BM-g-DPCL的基因表達水平高于DPCL和PCL。這些結果表明,BM-g-DPCL支架可以改善rBMSCs的增殖、血管生成和成骨分化以及特異性基質分泌。 圖2 體外細胞的增殖和分化 仿生基質加速rBMSCs體外遷移和體內內源性干細胞(ESCs)募集 通過跨孔模型證實支架對rBMSCs體外遷移行為的影響(圖3A)。結果表明,BM-g-DPCL組比DPCL和PCL組有更多的rBMSCs向trans-well的下腔遷移。半定量分析顯示,各處理組均促進了細胞遷移,且遷移細胞數量呈增加趨勢(BM-g-DPCL > DPCL > PCL > BK,圖3B,C)。醋酸溶解結晶紫在570 nm處的定量OD值證實了這一結果(圖3D)。rBMSCs遷移行為的改善可能是由于多酚或水凝膠吸附了功能蛋白或因子。 7天后提取體內植入支架,以評估家兔顱骨缺損部位內源性干細胞(ESCs)的募集情況(圖3E)。所有的干細胞標記物(CD29和CD90,圖3F)在BM-gDPCL組中均有顯著的陽性表達,而在PCL支架中幾乎沒有可見的干細胞,說明BM-g-DPCL支架可以刺激ESCs向缺陷區遷移。平均光密度(圖3G-H)證實了最強的熒光發生在BM-g-DPCL組。同時,CD31可見陽性染色(圖3F)證實了血管生長,ImageJ的半定量熒光強度分析顯示了BM-g-DPCL的最佳特征(圖3I)。簡而言之,BM-g-DPCL支架可以招募ESCs到缺陷部位,并刺激早期血管生成。 圖3 干細胞在體內的遷移和體外的募集 異位裸鼠模型中礦物質加速沉積 生物材料皮下植入為材料內部細胞的生長提供了適宜的微環境和豐富的營養供應,保證了在明確的影響因素下,材料誘導成骨細胞分化和干細胞礦化沉積的效果得以顯現。在這里,使用皮下植入物來評估28天后BALB/c裸鼠體內異位礦化和血管生成的潛力(圖4A)。通過微型計算機斷層掃描(CT)在BM-g-DPCL支架上沉積了最明顯的骨基質(圖4B),骨礦物質密度(BMD)、骨體積/組織體積(BV /TV)和骨表面積與組織體積比(BS/TV)參數證實了這種最佳的生物礦化沉積趨勢(圖4C-E)。與相對簡單的圓形細胞分布相反,CLSM顯示DPCL和BM-gDPCL存在不同程度的交織紡錘狀形態(圖4F)。SEM圖(圖4G)顯示纖維與基質交織的類骨磷灰石沉積較多(BM-g-DPCL > DPCL > PCL)。HE和Masson三色染色(圖4H-I)顯示BM-g-DPCL和DPCL支架含有細胞(HE中紫色點)和骨基質(藍色纖維),表明細胞增殖和生物礦化增強。CD31免疫染色的圖像和半定量結果(圖4J-L)存在顯著差異。與PCL和DPCL支架相比,BM-g-DPCL支架中出現的新生血管數量更多。Runx2免疫染色也顯示,移植細胞促進了所有組的骨形成,尤其是BM-g-DPCL支架(圖4K-M)。綜上所述,這些結果表明BM-g-DPCL支架可以促進體內異位血管形成和生物礦化。 圖4 裸鼠模型皮下植入各種支架后異位礦物沉積 支架內源性骨再生修復兔顱骨缺損 HE和Masson染色顯示,BM-g-DPCL組植入12周后,支架底部形成明顯連續完整的骨結構薄層(圖5A)。而PCL組和DPCL組僅修復了一小部分缺損體積。與BM-g-DPCL致密的再生界面相比,PCL和DPCL均存在宿主骨組織與支架之間的纖維組織,阻礙了骨組織的生長(圖5B、C)。 定量結果顯示,BM-gDPCL組骨體積/組織體積(BV /TV, 22.5±0.69%)顯著高于PCL和DPCL組(圖5D-E)。此外,BM-g-DPCL組也顯示出最好的骨形態學參數(圖5F-G),與上述HE和Masson染色結果一致,免疫組化染色圖像(圖5H-J)也均有證實,Image J顯示BM-g-DPCL組血管生成和成骨相關蛋白ANGPT、ColI、OPN和Runx2表達增強(圖5K-N)。這些結果表明BM-g-DPCL支架在促進血管化和長期骨再生方面具有更大的潛力。 圖5 線粒體呼吸鏈復合物I(A)、II(B)、III(C)、IV(D)和V(E)的酶活性測定 差異表達蛋白的比較揭示成骨分化機制 為了在蛋白質組學水平上了解不同支架在加速成骨過程中的作用,采用非標蛋白質組學方法獲得PCL、DPCL和BM-g-DPCL組在12周時的蛋白組成。通過主成分分析、差異表達蛋白維恩圖和聚類分析對三組樣本進行統計分析。結果表明,蛋白質組學數據可用于進一步分析。接下來,對差異表達蛋白(DEPs)進行火山圖分析(圖6A-B)。DPCL與PCL相比有519個DEPs上調,137個DEPs下調,BM-g-DPCL與DPCL相比有193個DEPs上調,170個DEPs下調。相對于PCL組,DPCL組顯著促進了細胞結合、細胞對氧化應激的反應和醌代謝過程(圖6C)。與DPCL組相比,BM-g-DPCL組顯著促進了細胞外基質的形成、軸突的發育和細胞結合(圖6D)。PDA涂層(圖6E)增加了細胞粘附和干細胞發育,并隨后增強成骨。BM-gDPCL通過促進細胞粘附、血管生成和潛在的炎癥調節來加速成骨(圖6F)。 差異蛋白質熱圖及蛋白質互作網絡闡明了這一過程(圖G-J)。含有生物活性水凝膠的BM-g-DPCL通過促進血管生成(MMP2、AGT、ITIH3、CSPG4)和細胞外基質(ECM)形成活性(FBLN1、ECM1、ECM2)以及骨重塑(SERPINH1、COL6A2、COL6A3)來促進骨生成。蛋白質組學數據分析與前期實驗結果一致,表明BM-g-DPCL組可通過整合類ECM生物活性水凝膠,加速整合素/肽/因子結合募集ESCs,進而促進ECM的構建和形成,進一步促進血管生成和成骨。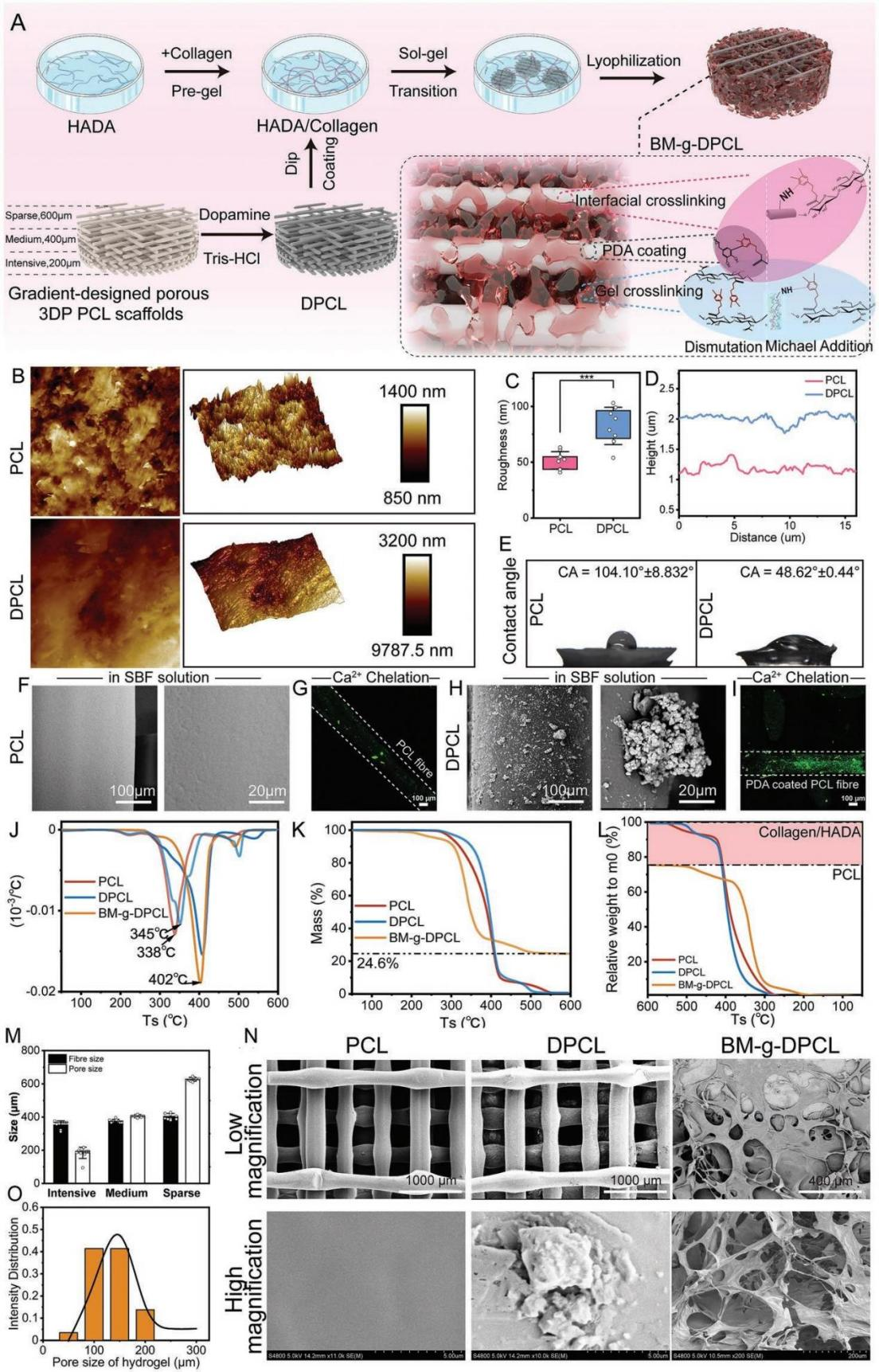
四、研究結論
本研究通過模仿骨基質的軟硬結合結構,利用多巴胺介導的仿生細胞外基質錨定聚多巴胺包被的3DP PCL支架(BM-g-DPCL),構建了一種化學鍵合結構。它促進了干細胞在體外的遷移、增殖和成骨分化,并加速了體內內源性干細胞的募集和快速血管生成。植入后,能在骨組織與種植體之間融合,誘導骨基質沉積。蛋白質組學證實細胞因子粘附、生物礦化、快速血管化和細胞外基質形成是臨床尺寸兔顱骨缺損重建滿意的主要因素。該策略為無生長因子/細胞骨再生支架提供了一種可選的設計思路。
原文索引: Liu Q, Chen M, Gu P, Tong L, Wang P, Zhu J, Xu Y, Lu G, Luo E, Liang J, Fan Y, Zhang X, Sun Y. Covalently Grafted Biomimetic Matrix Reconstructs the Regenerative Microenvironment of the Porous Gradient Polycaprolactone Scaffold to Accelerate Bone Remodeling. Small. 2023 May;19(19):e2206960.