
2021-08-31

發表期刊
Signal Transduction and Targeted Therapy
影響因子
18.187
文章題目:HIF-1α promotes SARS-CoV-2 infection and aggravates inflflammatory responses to COVID-19
發表期刊:Signal Transduction and Targeted Therapy
技術手段:RNA-Seq
派森諾生物與暨南大學攜手合作,于2021年8月在 《Signal Transduction and Targeted Therapy》上發表了關于新冠病毒感染機制的研究成果。
研究背景
嚴重急性呼吸系統綜合癥冠狀病毒2 (SARS-CoV-2) 引起了在全球數十億人中流行傳播的2019 年冠狀病毒病 (COVID-19)。病毒引起的細胞因子風暴是導致COVID-19患者病情嚴重的主要原因。而年齡、性別和既往存在的共病(包括癌癥、糖尿病和心血管疾病)是COVID-19患者的主要危險因素。代謝途徑,特別是糖代謝,在COVID-19患者的預后中發揮著重要作用。治療COVID-19的常見方法包括抗感染、抗炎和抗細胞因子風暴治療,然而目前還沒有治療病毒感染的特效藥。因此,我們迫切需要了解SARS-CoV-2的感染和發病機制以及宿主的免疫和炎癥反應。
缺氧誘導因子1α(HIF-1α)是代謝、細胞增殖和血管生成等生理功能中起作用的關鍵調節因子。HIF-1α也是糖酵解和炎癥反應中的重要激活因子,這意味著HIF-1α對COVID-19的發病機制存在一定的影響。了解SARS-CoV-2的發病機制,尋找潛在的抗病毒藥物,非常值得關注。本研究基于RNA測序和臨床樣本的分析,探討SARS-CoV-2感染及發病的分子機制,為研制病毒感染特效藥奠定理論基礎。
研究思路
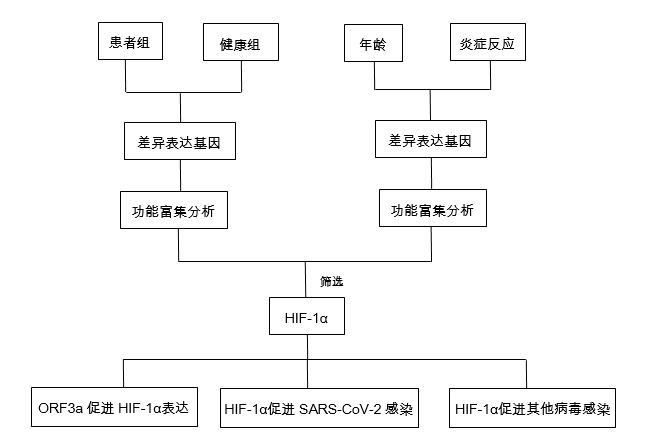
研究結果
1. COVID-19患者的免疫和代謝通路失調
從RNA-seq數據中鑒定出的18,483個基因中,有659個基因下調,856個基因上調。對患者和健康個體之間差異基因進行GO富集分析,富集到的GO條目包括膜功能、免疫反應、內質網定位和代謝途徑。同時顯示了患者和健康個體pbmc之間與基因失調相關KEGG通路的改變,結果發現在SARS-CoV-2感染后,代謝、免疫和細胞因子的信號通路受到調控。特別是TNF信號、NF-κB信號、HIF-1信號、代謝和免疫通路表達上調。
同時研究了年齡和炎癥反應之間的聯系,發現老年組的HIF-1信號通路和免疫通路均表達上調,表明HIF-1信號通路是老年患者與炎癥反應相關的關鍵調控因子之一。另外,在COVID-19患者的PBMCs中,有10個基因,包括缺氧誘導因子1α(HIF-1α)和6-磷酸果糖-2-激酶/果糖-2,6-雙磷酸酶3(PFKFB3)、兩個糖酵解相關基因,以及其他與細胞增殖、免疫反應和代謝相關的基因表達上調。總的來說,SARS-CoV-2感染與COVID-19患者血液樣本中的HIF-1α、免疫和代謝的途徑高度相關。
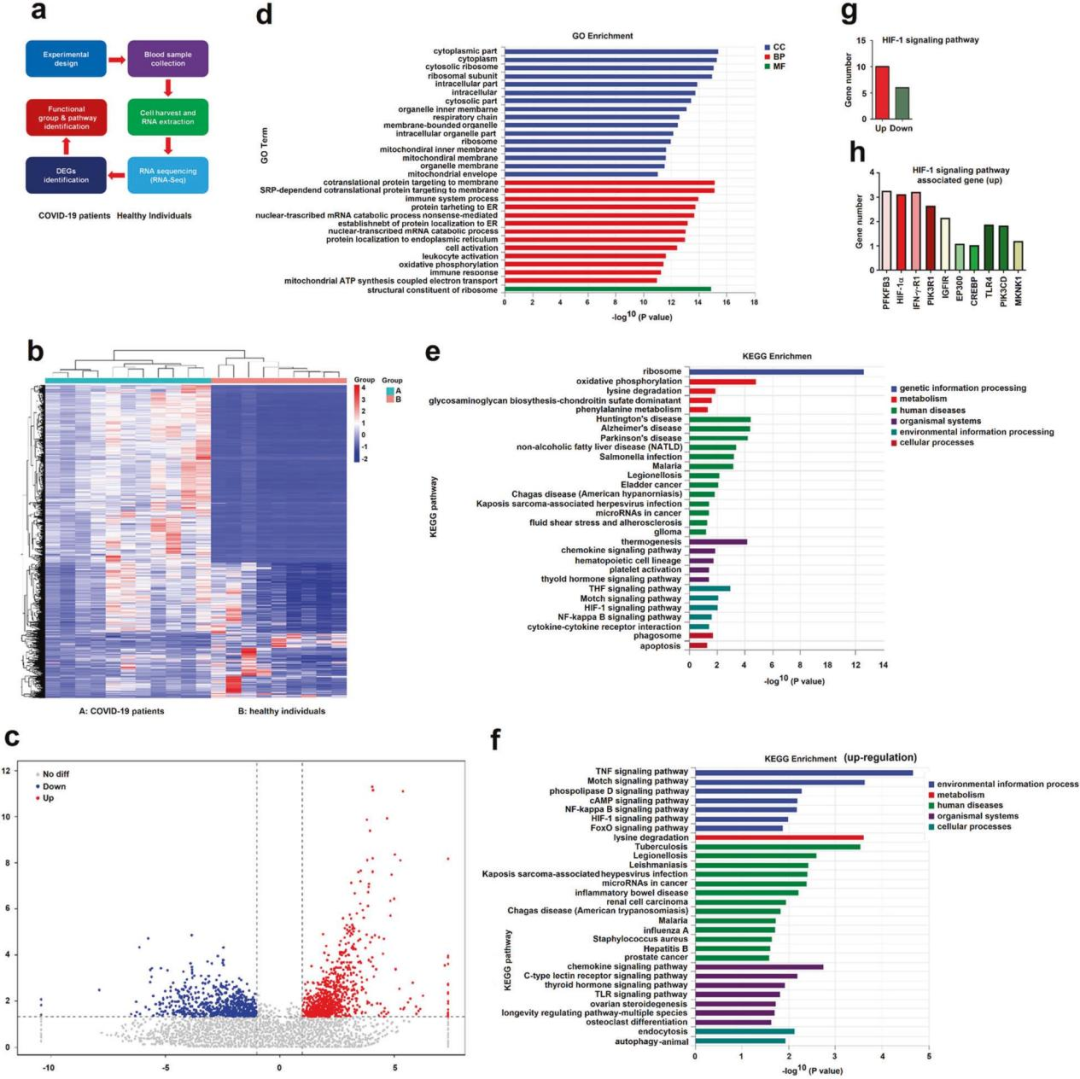
圖1 COVID-19患者的免疫和代謝途徑失調
2.老年COVID-19患者炎癥反應過度,死亡率高
對SARS-CoV-2感染后患者體內參與免疫和炎癥反應的蛋白質水平進行研究。結果顯示,與健康組相比,患者組中IL-6、IL-10和TNF-α蛋白水平顯著改變,表明SARS-CoV-2會引起患者pbmc的炎癥反應。對年輕和老年患者進行研究表明老年人更容易受到感染SARS-CoV-2。與年輕健康個體相比年輕患者分泌的IL-2、IL-6、IL-10和TNF-α蛋白水平差異不大,但老年患者與老年健康個體相比分泌蛋白水平明顯升高。此外,與年齡在50歲以下的患者相比,65歲以上患者的死亡病例數要高得多。這些結果表明,SARS-CoV-2感染會使老年患者體內產生過度的促炎細胞因子,從而可能導致病情加重甚至患者的死亡。
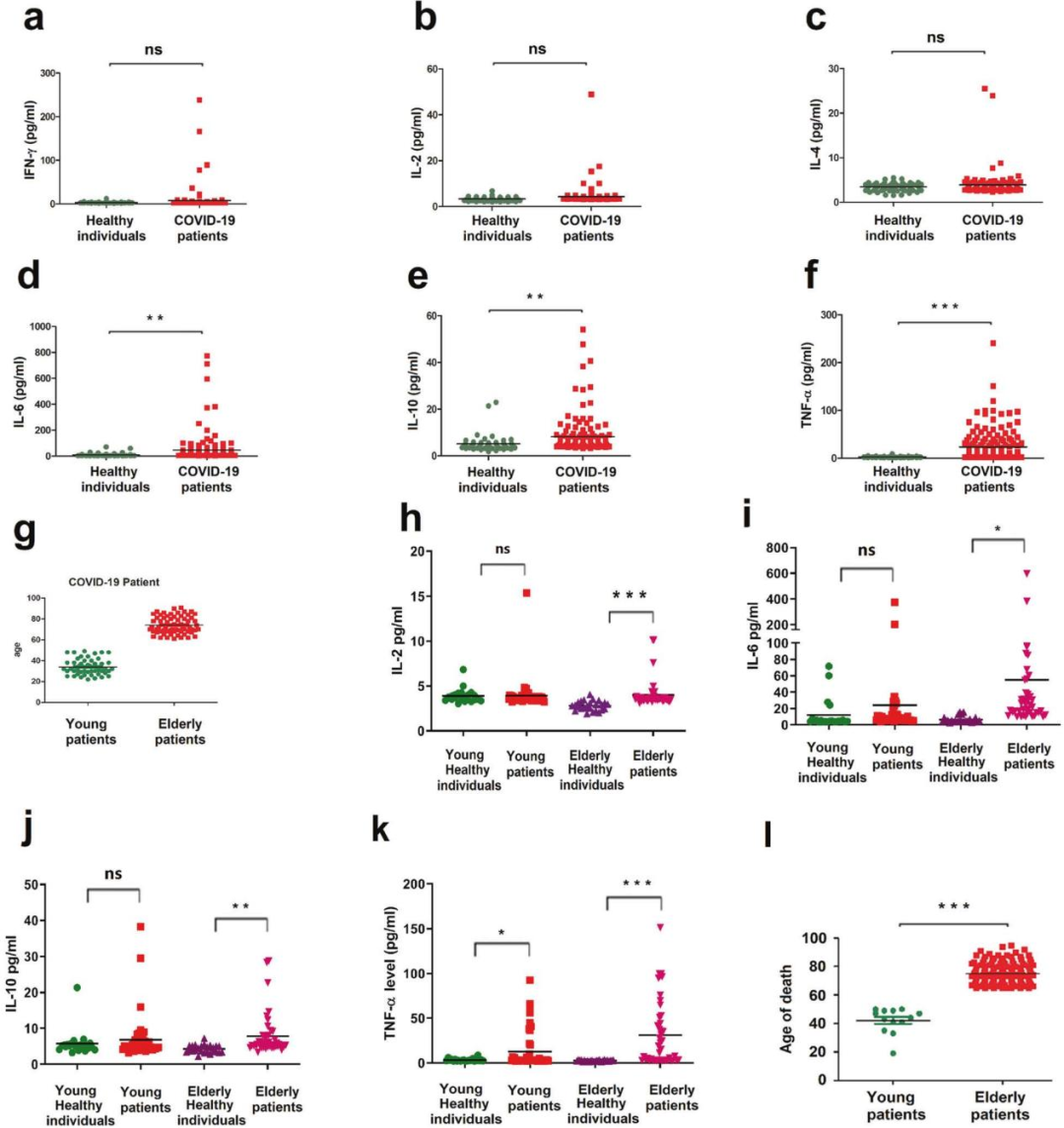
圖2 老年患者表現出過度的炎癥反應和高死亡率
3.SARS-CoV-2感染可誘導HIF-1α和促炎細胞因子
對SARS-CoV-2誘導的免疫炎癥反應的分子機制進行研究。RNASeq數據顯示,在 COVID-19 患者的血液樣本中,氧通路和 HIF-1α 信號通路的HIF上調,表明HIF-1α可能在調節病毒感染時的免疫和炎癥反應中起著重要作用。與健康個體相比,患者的pbmc中HIF-1α和IL-1β的mRNA水平要高得多;而老年健康個體的HIF-1α的mRNA水平明顯高于年輕健康個體。同時構建了病毒感染模型來驗證SARS-CoV-2感染對HIF-1α和炎癥細胞因子的誘導作用。
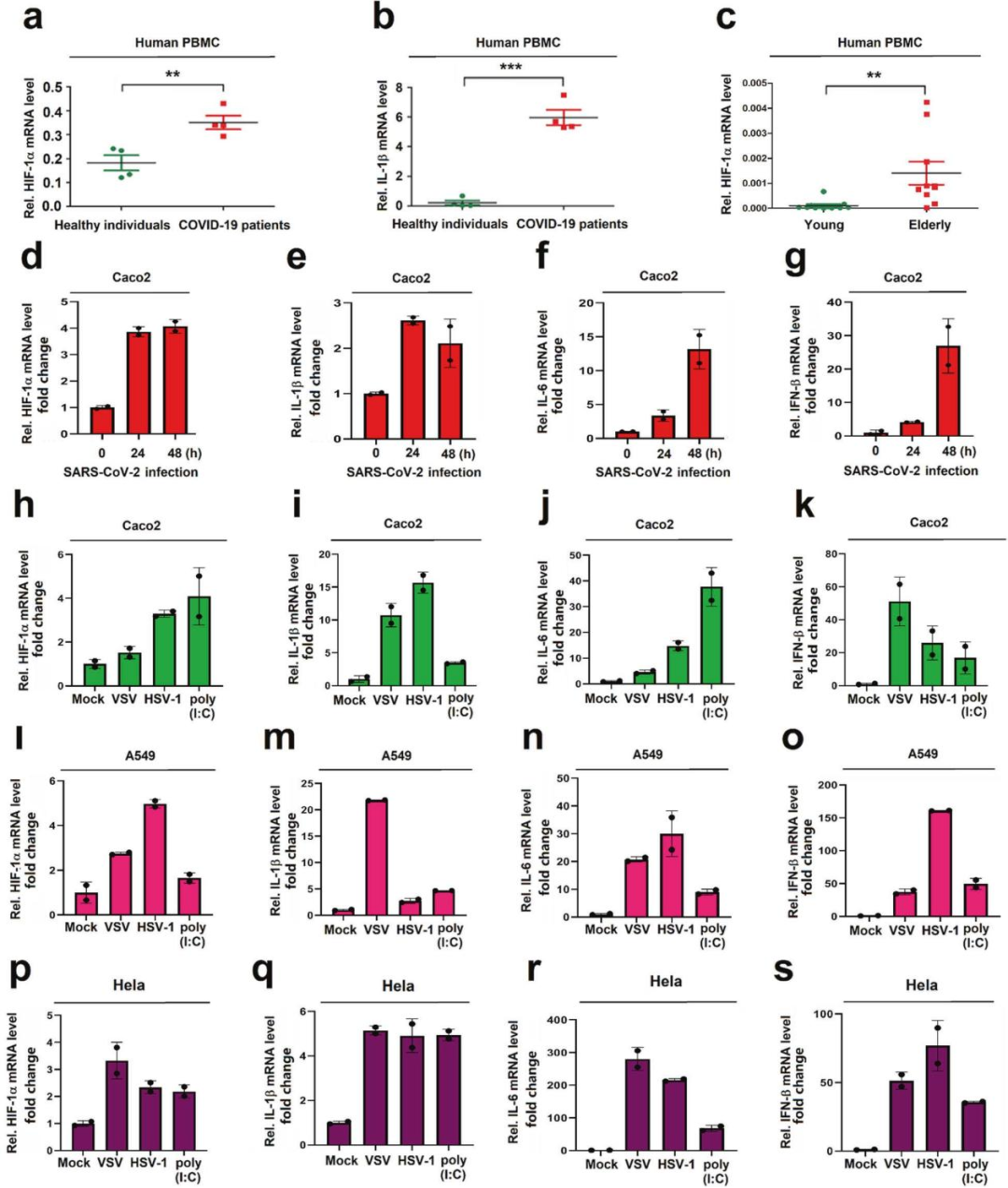
圖3 HIF-1α和炎癥因子是由SARS-CoV-2感染誘導
4.ORF3a通過Mito-ROS信號通路促進HIF-1α的產生和炎癥反應
進一步探討SARS-CoV-2誘導HIF-1α表達和炎癥反應的機制。通過在細胞中轉染攜帶病毒的質粒并用氯化鈷(HIF-1α誘導劑)處理,結果發現ORF3a增強了氯化鈷處理及病毒感染的細胞中HIF-1α的mRNA的表達,且ORF3a能通過激活HIF-1α促進促炎細胞因子的產生。
先前的研究報道,線粒體來源的活性氧(Mito-ROS)是HIF-1α的強誘導劑,SARS-CoV-2誘導ROS和HIF-1α的產生。研究發現ORF3a降低了線粒體膜電位,而ORF3a促進了ROS的生成,表明ORF3a誘導線粒體損傷。因此,我們提出,在SARS-CoV-2感染時,ORF3a誘導Mito-ROS的產生,激活HIF-1α,進而增強病毒感染加重炎癥反應。
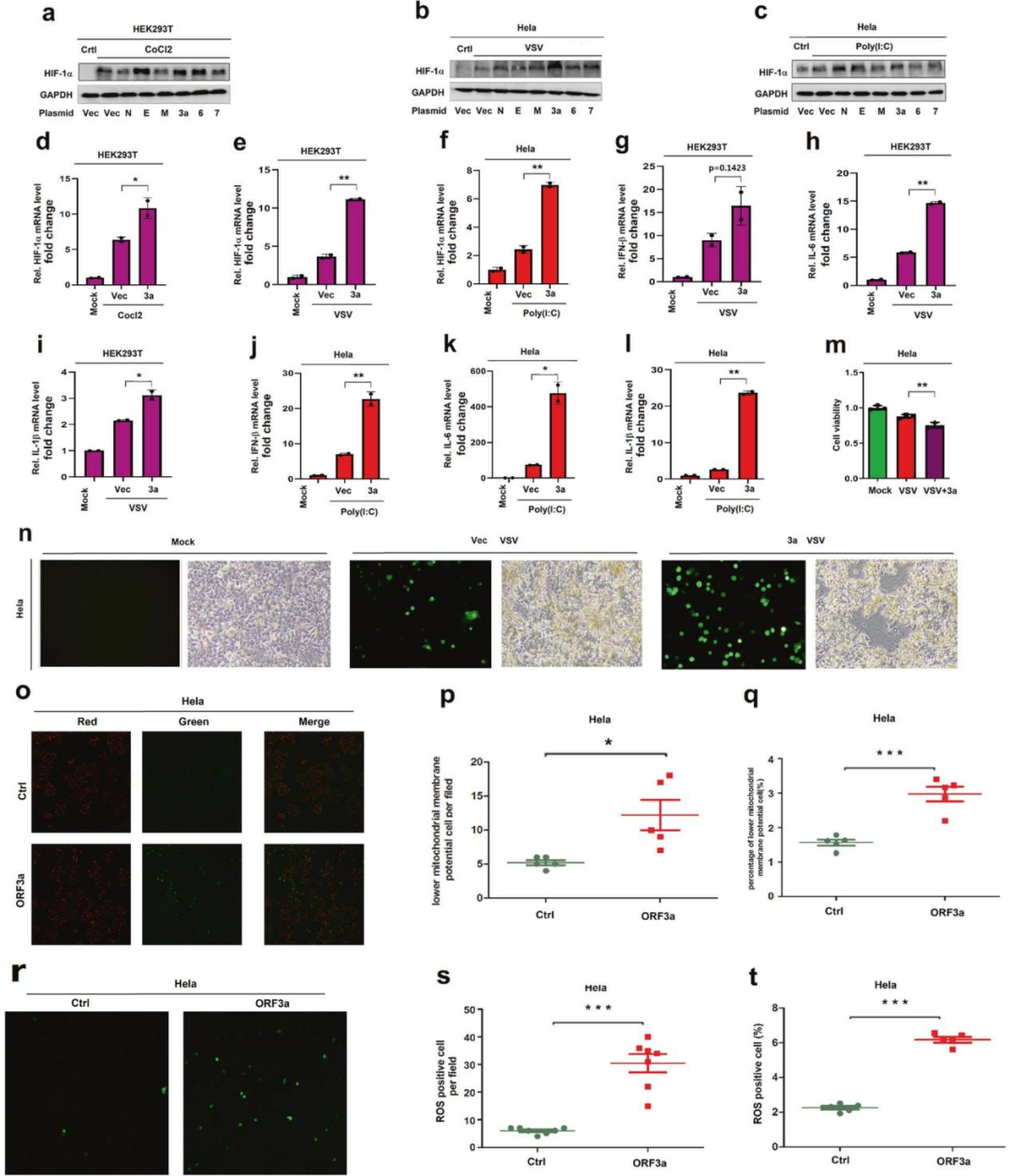
圖4 SARS-CoV-2 ORF3a促進HIF-1α的產生和炎癥反應
5.HIF-1α促進SARS-CoV-2感染和炎癥反應
考慮到HIF-1α在生物過程中的重要作用,推測HIF-1α可能在調節SARS-CoV-2復制和免疫炎癥反應中發揮重要作用。結果證實,HIF-1α在調控SARS-CoV-2復制中發揮了積極作用,HIF-1α的誘導促進炎性細胞因子,而抑制 HIF-1α會抑制炎性細胞因子。
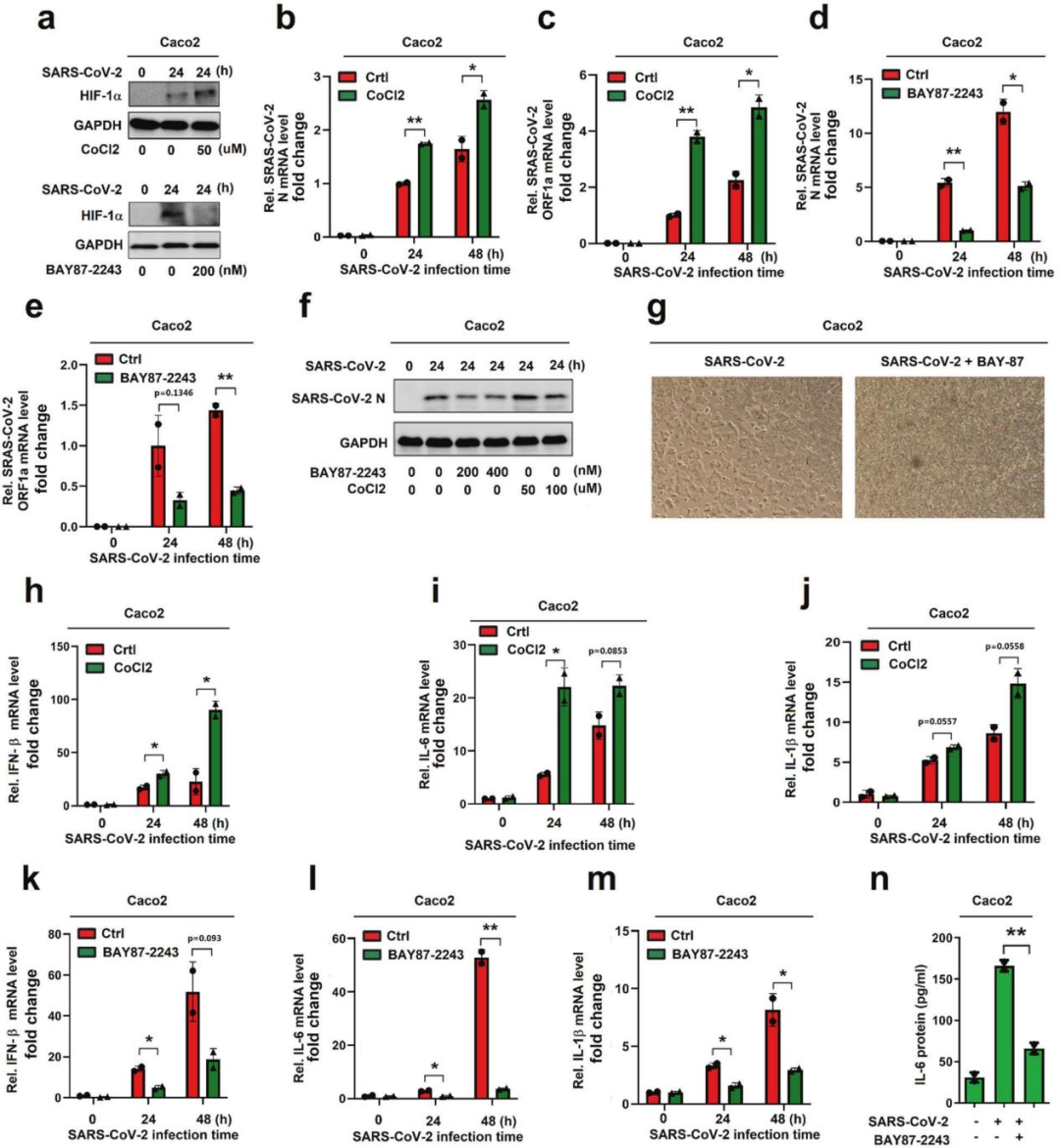
圖5 HIF-1α促進SARS-CoV-2感染和炎癥反應
6.HIF-1α在促進病毒感染中發揮著廣泛的作用
由于HIF-1α促進SARS-CoV-2復制,并在多種病毒感染時被誘導,因此研究了HIF-1α對其他病毒感染的影響。結果表明,抑制HIF-1α可抑制VSV和HSV-1的感染和炎癥細胞因子的產生。
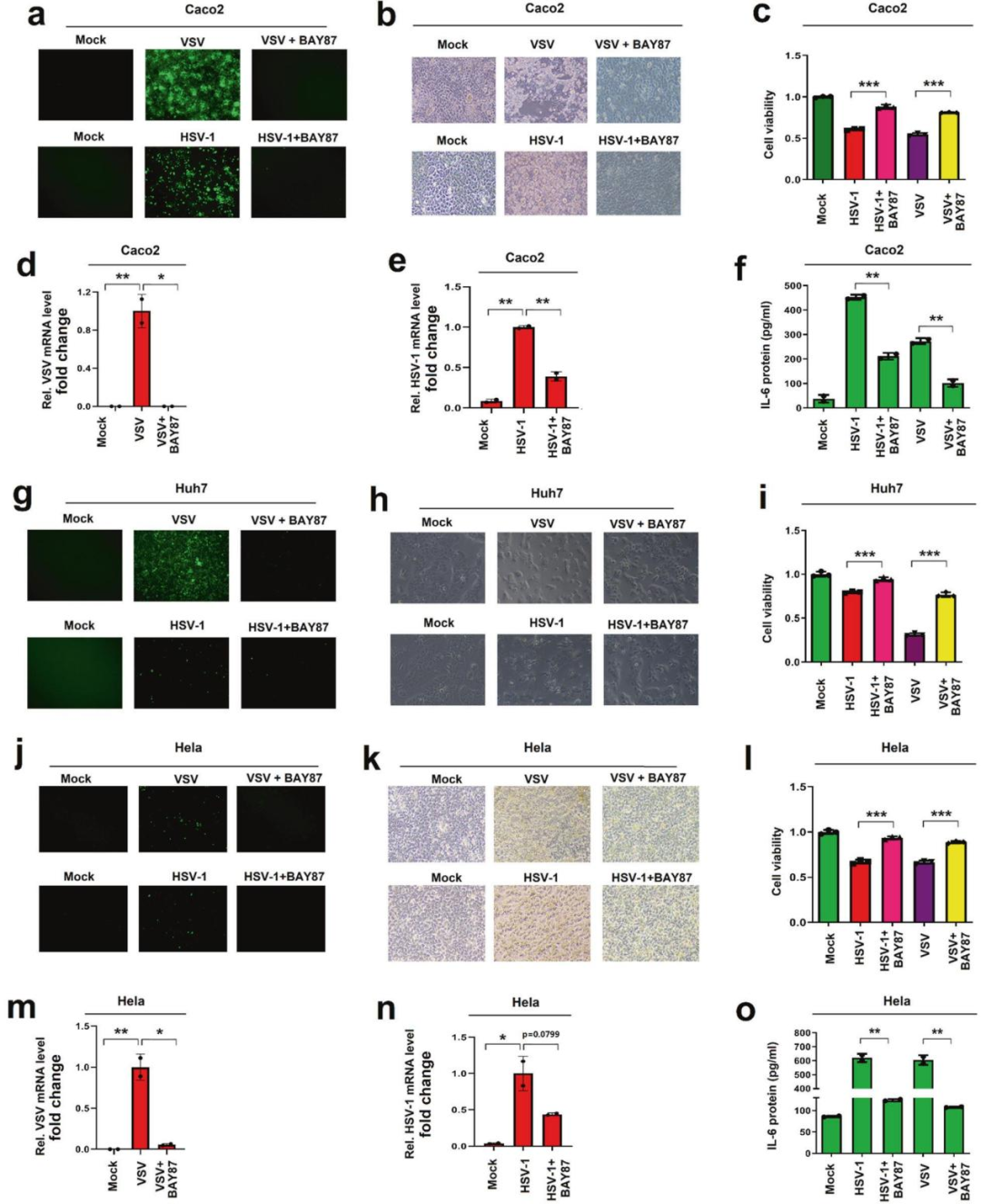
圖6 HIF-1α在促進病毒感染方面發揮著廣泛的作用
文章小結
嚴重急性呼吸系統綜合征冠狀病毒2(SARS-CoV-2)誘導的細胞因子風暴是2019冠狀病毒病(COVID-19)的主要病理特征,也是COVID-19預后的關鍵決定因素。了解SARS-CoV-2誘導的細胞因子風暴的機制對COVID-19的控制至關重要。本研究的RNA測序結果顯示,COVID-19患者的HIF-1α信號通路、免疫應答和代謝通路發生失調。臨床分析表明,老年患者出現HIF-1α的產生、炎癥反應和高死亡率。HIF-1α和促炎細胞因子在患者和感染細胞中被誘導。有趣的是,SARS-CoV-2的ORF3a誘導線粒體損傷和Mito-ROS的產生,促進HIF-1α的表達,進而促進SARS-CoV-2感染和細胞因子的產生,進而加重病毒感染和炎癥反應。并且HIF-1α也廣泛促進其他病毒的感染。因此,HIF-1α是SARS-CoV-2感染和炎癥反應的關鍵激活因子,也是病毒誘導的炎癥性疾病和COVID-19的潛在治療靶點。
本研究的數據分析工作由上海派森諾生物科技有限公司完成。
原文索引
Tian, M., Liu, W., Li, X. et al. HIF-1α promotes SARS-CoV-2 infection and aggravates inflammatory responses to COVID-19. Sig Transduct Target Ther 6, 308 (2021).
更多新聞資訊,請關注派森諾官網