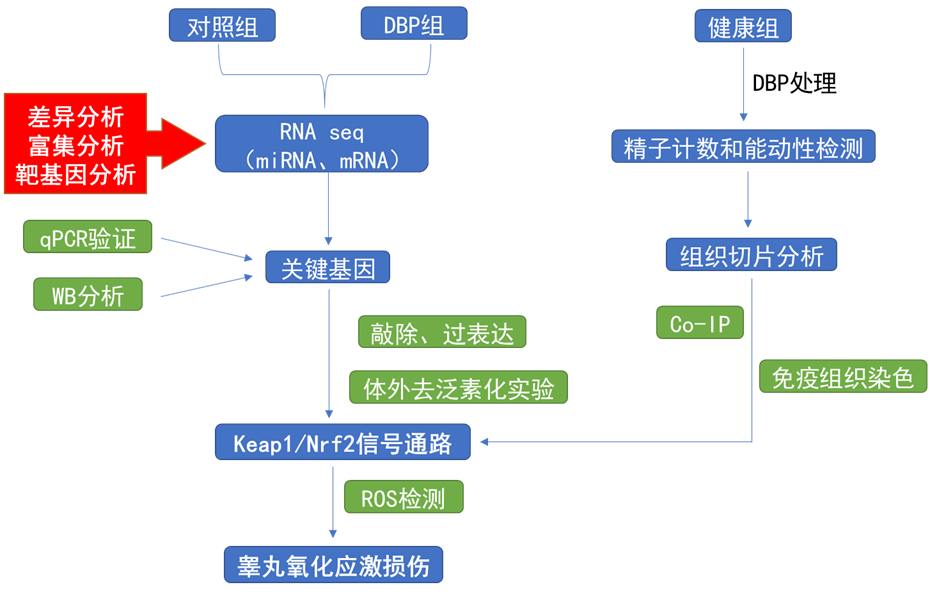
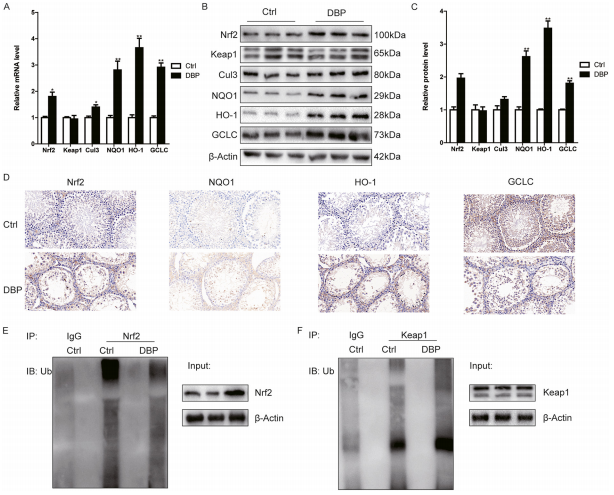
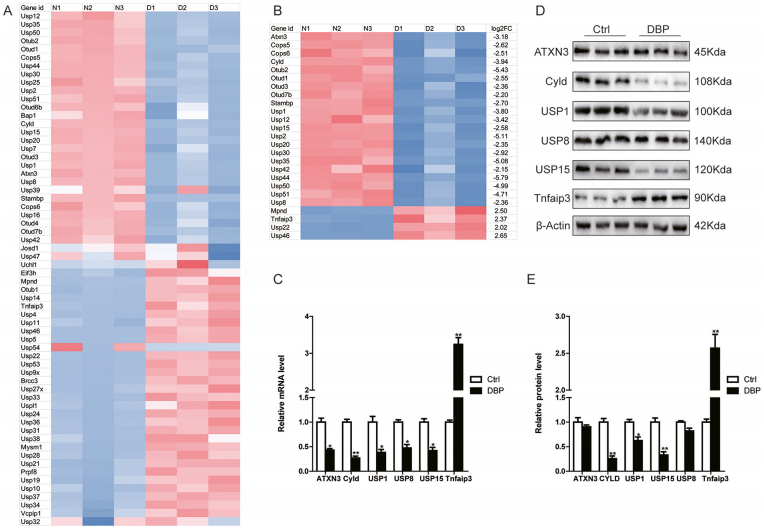
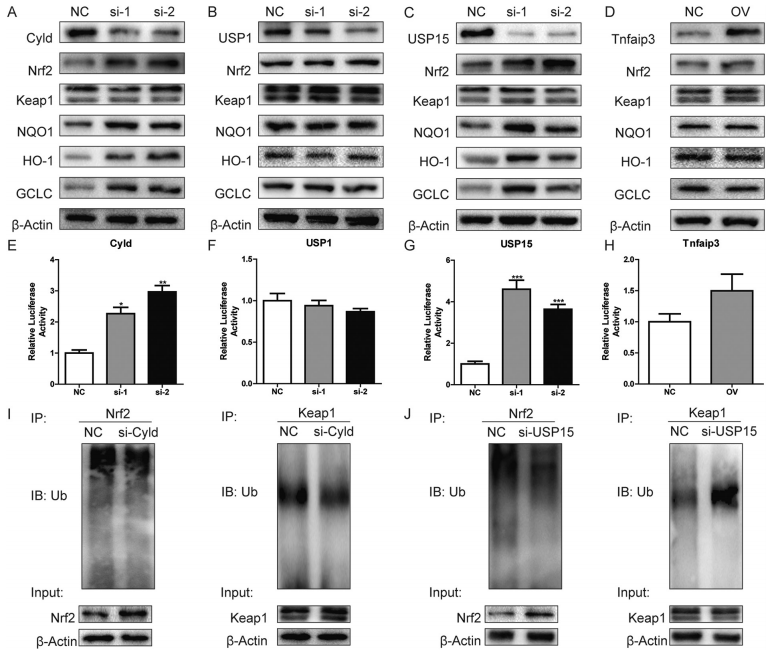
- 首頁
-
科研服務(wù)
轉(zhuǎn)錄組
單細(xì)胞組
表觀基因組學(xué)
代謝組
微生物基因組
動植物基因組
三代測序服務(wù)
常規(guī)分子實驗
常規(guī)測序與合成
-
健康醫(yī)學(xué)
新型冠狀病毒核酸檢測
- 派森諾基因云
-
技術(shù)平臺
NGS測序平臺
單細(xì)胞空轉(zhuǎn)平臺
- 市場活動
- 關(guān)于我們