
2019-08-13
派森諾生物與華中科技大學同濟醫院攜手合作,于2019年6月在《Molecular Therapy: Nucleic Acid 》上發表了基于miRNA的糖尿病性心肌病臨床治療新思路,影響因子5.919。
研究背景
心血管疾病是糖尿病患者嚴重的并發癥之一,而目前常規的抗高糖治療手段對于糖尿病性心肌病(DCM)患者的心力衰竭無顯著療效。越來越多的研究表明,線粒體功能障礙誘導生成的活性氧(ROS)可能是糖尿病性心肌病的主要誘因;此外有實驗數據證實,miRNA能夠轉位到線粒體,可對線粒體基因的表達起正調控作用。然而,線粒體miRNA在糖尿病性心肌病中的作用目前尚無定論。
基于此,本研究假設線粒體miRNA表達量的改變可能與糖尿病性心肌病的病情發展有關,以db/db小鼠(科研用2型糖尿病小鼠)為研究對象,利用miRNA-mRNA測序及聯合分析手段,進行了針對糖尿病患者心衰治療的線粒體生物學研究。
研究結果
1、線粒體Cytb的下調表達導致db/db小鼠心臟ROS增加
通過比對db/db小鼠和正常小鼠的心臟切片可發現,前者的ROS量顯著增加(圖1)。由于線粒體是ROS的主要來源,接下來通過Western blot和Real-time PCR (RT-qPCR)分別檢測db/db小鼠線粒體各亞基的表達情況。結果顯示,從轉錄水平看,db/db小鼠線粒體電子呼吸鏈的各亞基mRNA表達量無顯著差異(圖2);而從蛋白水平看,db/db小鼠線粒體ETCIII上的細胞色素b(Cytb)表達量顯著低于對照組(圖3)。
為證實低表達Cytb與高表達ROS間的關系,以大鼠心肌細胞H9C2研究對象,對包括Cytb在內的、由mtDNA編碼的多個線粒體亞基進行了特異性siRNA轉染實驗。結果表明,僅si-Cytb處理導致細胞內ROS量顯著上升(圖4)。這些數據表明Cytb在ROS生成中起著關鍵作用。因此選擇Cytb作為對象,進行深入研究。
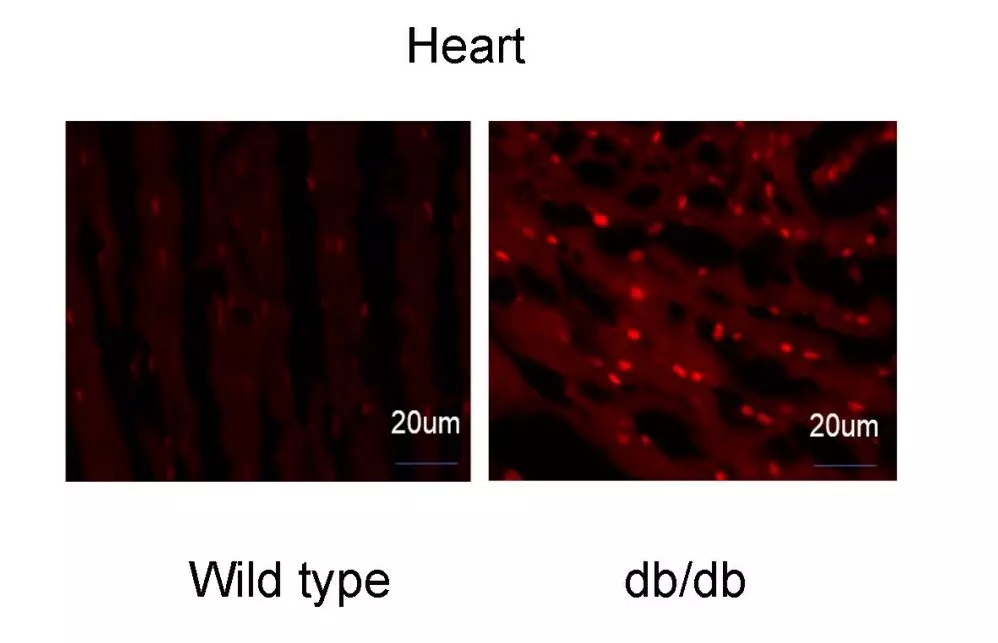
圖1 用DHE探針在db/db小鼠冷凍心臟切片中檢測ROS的情況(n=3)
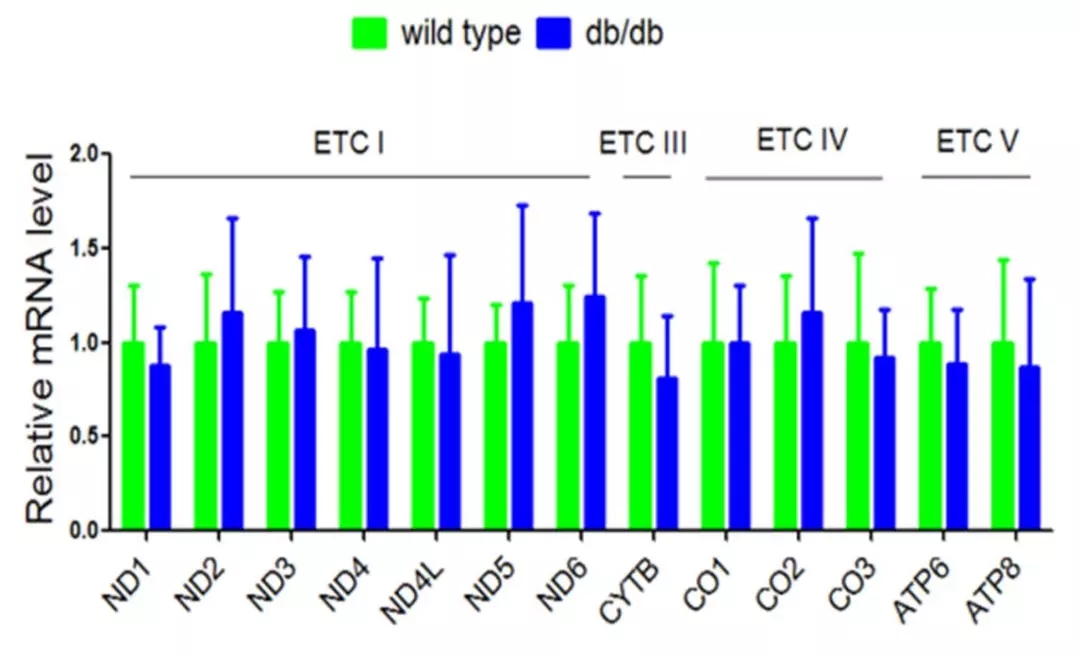
圖2 RT-qPCR檢測db/db小鼠心臟中ETC各亞基的mRNA表達水平
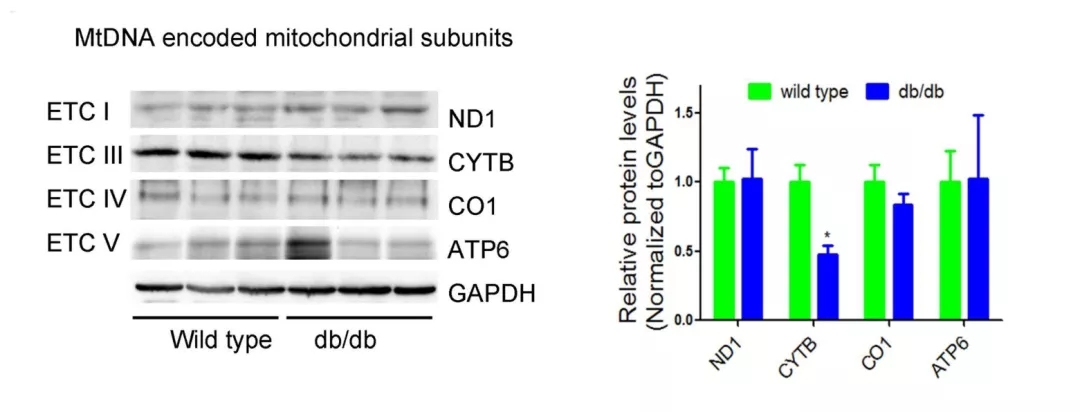
圖3 Western blot檢測db/db小鼠心臟中ETC各亞基的蛋白表達水平
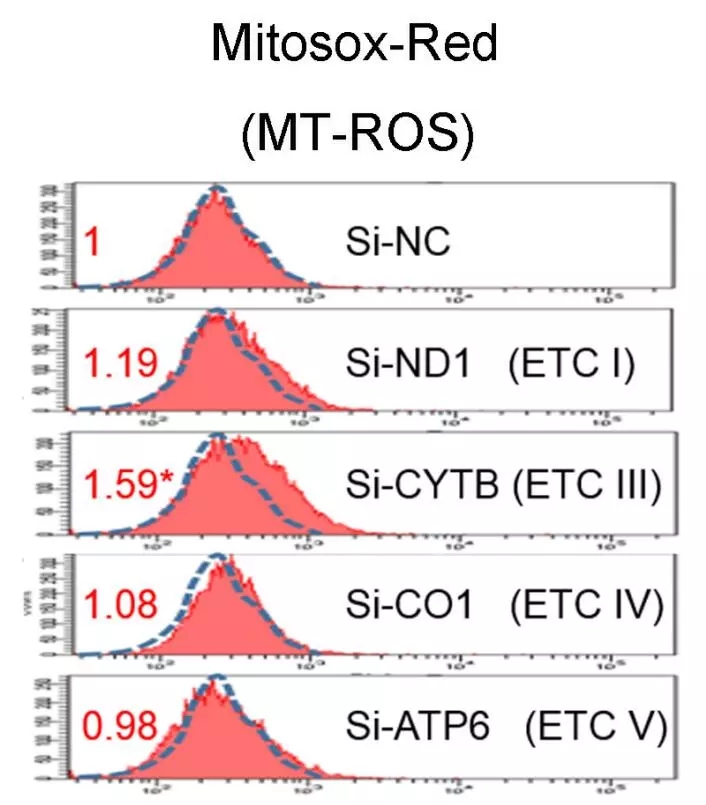
圖4 用MitoSox Red檢測si-ND1、si-Cytb、si-COI和si-ATP6處理后H9c2細胞的線粒體ROS水平
2、轉錄組測序揭示Cytb在心肌細胞中的功能
以正常的人心肌細胞為對照組,si-Cytb處理的心肌細胞為處理組(n=3),通過轉錄組測序進一步研究Cytb在心肌細胞中的功能。Heatmap顯示兩種心肌細胞的基因表達模式存在明顯差異(圖5A),火山圖顯示兩種細胞間的差異基因多達數百個(圖5B)。KEGG pathway富集分析結果表明,si-Cytb處理的心肌細胞中TNF信號通路、細胞因子-細胞因子受體相互作用通路、NF-kappa B信號通路顯著上調(圖5C),而細胞周期、cAMP信號通路、鈣信號通路顯著下調(圖5D)。有研究表明,腫瘤壞死因子信號通路,如TNF和NF-kappa B等,是糖尿病性心肌病進展的重要調控因子。這些數據暗示Cytb在糖尿病性心肌病中發揮著潛在作用。
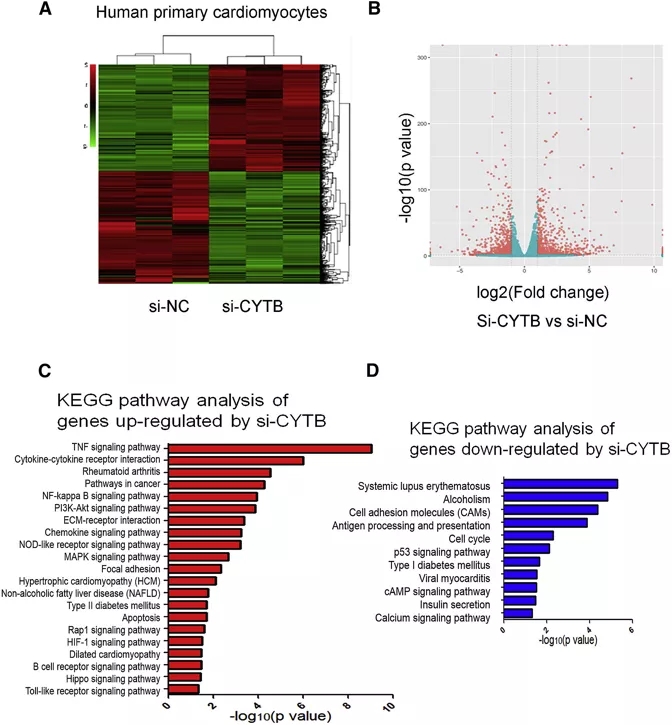
圖5 應用mRNA-seq分析Cytb在人心肌細胞中的功能
A:兩種處理下的心肌細胞基因雙向聚類熱圖
B:兩種處理下的心肌細胞差異基因火山圖
C:si-Cytb處理心肌細胞的上調基因KEGG pathway富集分析結果
C:si-Cytb處理心肌細胞的下調基因KEGG pathway富集分析結果
3、miRNA-mRNA聯合分析尋找可作用于Cytb的miRNA
為尋找以Cytb為靶標的miRNA,以db/db小鼠的心臟和心臟線粒體為處理組,正常小鼠的相應樣本為對照組(n=3)進行miRNA測序。結果顯示,db/db小鼠的心臟樣本中,有24個miRNA上調表達,24個miRNA下調表達(表1),而其心臟線粒體樣本中,僅有14個miRNA下調表達(表2)。基于線粒體翻譯中miRNA的正向調控作用,選擇下調的miRNA作為預測指標,分別與人、大鼠、小鼠的Cytb mRNA序列進行比對,篩選出了4個以Cytb轉錄本為靶標的miRNA(圖6)。
為進一步確認候選線粒體miRNA對Cytb表達的影響,分別用這4種miRNA轉染不同類型的心肌細胞,發現僅有兩種miRNA:let-7b-5p和miR-92a-2-5p,會導致Cytb上調表達;此外過表達miR-92a-2-5p或let-7b-5p可降低心肌細胞的ROS水平。這些數據強有力地證實了miR-92a-2-5p和let-7b-5p可正向調控Cytb的表達,從而降低ROS量。
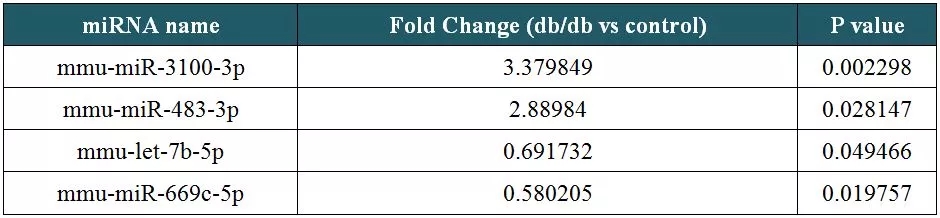
表1:小鼠心臟樣品中差異miRNA數據(部分)
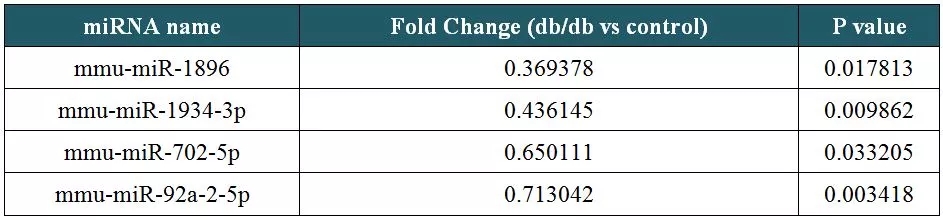
表2:小鼠心臟線粒體樣品中差異miRNA數據(部分)
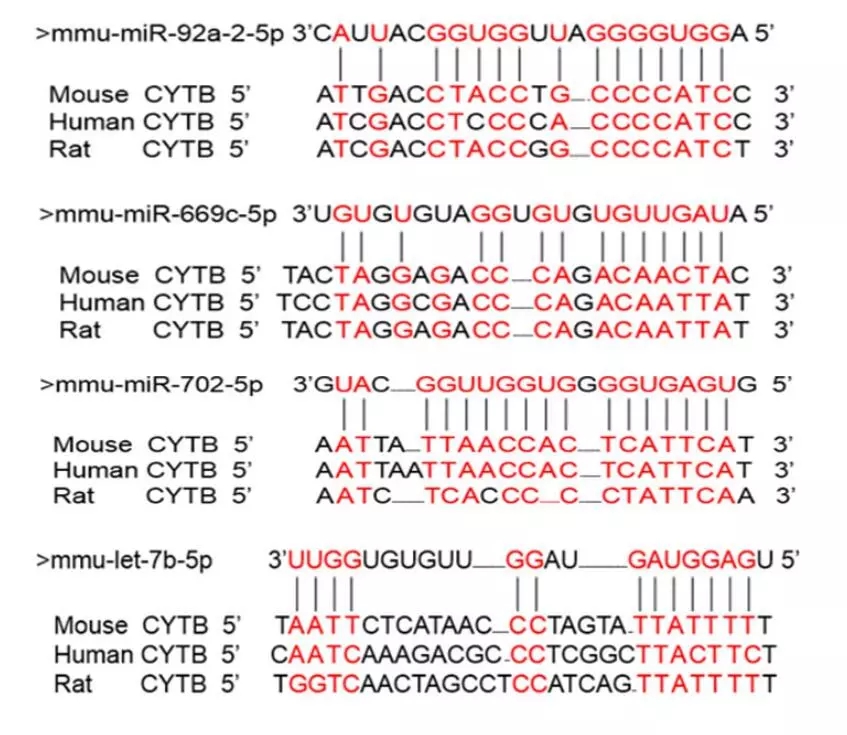
圖6 候選miRNA(miR-92a-2-5p、let-7b-5p、miR-669c-5p和miR-702)與不同生物Cytb mRNA的序列比對結果
4、活體驗證結合富集分析明確兩種miRNA的作用機制
為明確分別達miR-92a-2-5p和let-7b-5p是否能夠減輕糖尿病性心肌病的癥狀,用db/db小鼠模型進行生物活體驗證。結果表明,僅轉染miR-92a-2-5p可緩解db/db小鼠的心臟舒張功能障礙,而轉染let-7b-5p卻無效果,這似乎與miRNA-mRNA聯合分析的結果相悖。
為解釋這一現象,對let-7b-5p的靶基因進行了富集分析。結果表明,MAPK信號相關基因,如IRS1、AKT1、IGF1可能受let-7b-5p調控(圖7),Western blot進一步證實let-7b-5p可導致心肌細胞的IRS1下調表達;IRS是一種胰島素受體底物,它的降低會導致脂質沉積增加,從而加重心臟負擔。換言之,let-7b-5p降低心肌細胞ROS的效果與其增加心肌脂質沉積的效果相互“抵消”,最終造成該miRNA對心臟舒張功能障礙無緩解效果。miR-92a-2-5p和let-7b-5p在糖尿病性心肌病中發揮的作用可用圖8模型說明。
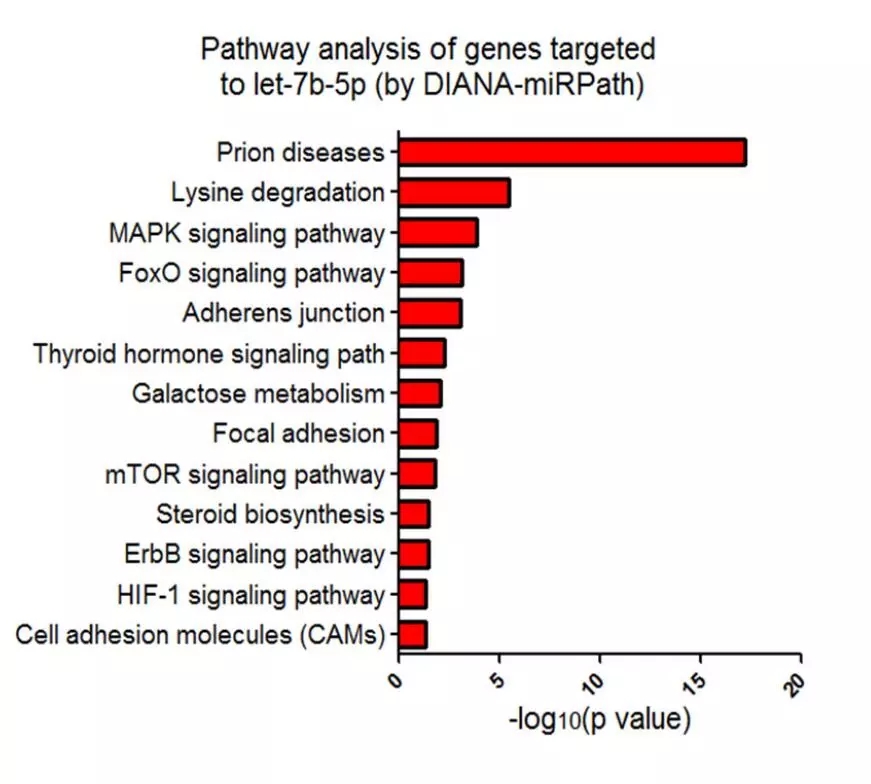
圖7 基于DIANA-miRPath對let-7b-5p的潛在靶向基因進行KEGG Pathway富集分析結果
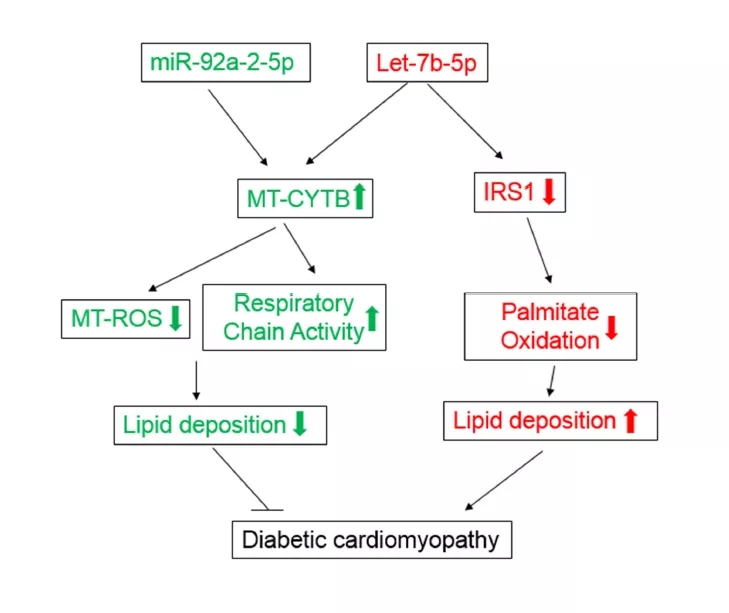
圖8 miR-92a-2-5p和let-7b-5p在糖尿病性心肌病中的作用模式圖
文章小結
該研究通過mRNA-miRNA測序及聯合分析,揭示了miR-92a-2-5p在線粒體翻譯中的積極作用。具體而言,該miRNA的過表達可增強線粒體Cytb的翻譯,從而減少ROS生成和脂質沉積,最終緩解心臟舒張功能障礙。該結果為發展基于miRNA的糖尿病性心肌病治療手段提供了理論基礎。
本研究的測序和數據分析工作由上海派森諾生物科技股份有限公司完成。
原文索引
Li HP, Dai BB, Fan JH, et al. The different roles of miRNA-92a-2-5p and let-7b-5p in mitochondrial translation in db/db mice [J]. Molecular Therapy:Nucleic Acid, 2019, 17: 424-435.