scGRO-seq——新型單細(xì)胞新生RNA測(cè)序揭示全基因組協(xié)調(diào)轉(zhuǎn)錄
2024-07-20

轉(zhuǎn)錄是基因表達(dá)的關(guān)鍵調(diào)控步驟,是一個(gè)內(nèi)在的不連續(xù)動(dòng)態(tài)過(guò)程,其調(diào)控涉及核心啟動(dòng)子元件、轉(zhuǎn)錄因子和增強(qiáng)子,具有短爆發(fā)和長(zhǎng)沉默期的特點(diǎn)。增強(qiáng)子是在發(fā)育和疾病過(guò)程中對(duì)基因調(diào)控和細(xì)胞識(shí)別控制至關(guān)重要的遠(yuǎn)端基因組元件,增強(qiáng)子在轉(zhuǎn)錄過(guò)程中會(huì)轉(zhuǎn)錄表達(dá)非編碼增強(qiáng)子RNA(eRNA),越來(lái)越多的研究表明eRNA在基因調(diào)控中發(fā)揮重要作用,而且eRNA對(duì)細(xì)胞類(lèi)型和狀態(tài)具有高度特異性,可以通過(guò)研究eRNA轉(zhuǎn)錄表達(dá)而將其作為診斷標(biāo)志物或治療靶點(diǎn),因此研究增強(qiáng)子對(duì)于解析細(xì)胞周期、發(fā)育和疾病期間的轉(zhuǎn)錄調(diào)控機(jī)制至關(guān)重要。
新生RNA(nascent RNA)是指正在轉(zhuǎn)錄的RNA分子,通過(guò)新生RNA研究基因的實(shí)時(shí)轉(zhuǎn)錄活動(dòng)狀態(tài),揭示轉(zhuǎn)錄調(diào)控機(jī)制。新生RNA不僅具有半衰期短、豐度低的特征,而且不具有Poly(A)尾,只能從豐富的總細(xì)胞 RNA 中選擇性標(biāo)記和富集新生RNA。目前常規(guī)單細(xì)胞測(cè)序雖然能研究細(xì)胞之間異質(zhì)性,但平均了單個(gè)細(xì)胞的不連續(xù)轉(zhuǎn)錄,無(wú)法捕獲活躍的轉(zhuǎn)錄過(guò)程,使得在單細(xì)胞分辨率下對(duì)轉(zhuǎn)錄動(dòng)力學(xué)和研究增強(qiáng)子-基因關(guān)系具有一定挑戰(zhàn)性。
2024年6月5日,來(lái)自麻省理工學(xué)院的Phillip A. Sharp研究團(tuán)隊(duì)在Nature期刊上發(fā)表一篇Single-cell nascent RNA sequencing unveils coordinated global transcription的研究文章,文中介紹了一種新型單細(xì)胞新生RNA測(cè)序方法(scGRO-seq),通過(guò)點(diǎn)擊化學(xué)(click chemistry)定量評(píng)估單個(gè)細(xì)胞的全基因組新生轉(zhuǎn)錄活動(dòng)。作者將scGRO-seq應(yīng)用于小鼠胚胎干細(xì)胞,通過(guò)分析獲得細(xì)胞基因和增強(qiáng)子轉(zhuǎn)錄動(dòng)態(tài)的全面視圖,量化了轉(zhuǎn)錄爆發(fā)動(dòng)力學(xué)和難以檢測(cè)特異性基因的細(xì)胞周期期間的轉(zhuǎn)錄動(dòng)力學(xué),同時(shí)研究發(fā)現(xiàn)在增強(qiáng)子開(kāi)始轉(zhuǎn)錄激活時(shí)間早于相關(guān)基因轉(zhuǎn)錄激活。總而言之,scGRO-seq可以填補(bǔ)轉(zhuǎn)錄時(shí)間控制以及增強(qiáng)子-基因相關(guān)功能研究空白,同時(shí)為深入探究細(xì)胞周期、發(fā)育和疾病中的基因調(diào)控機(jī)制提供新平臺(tái)。
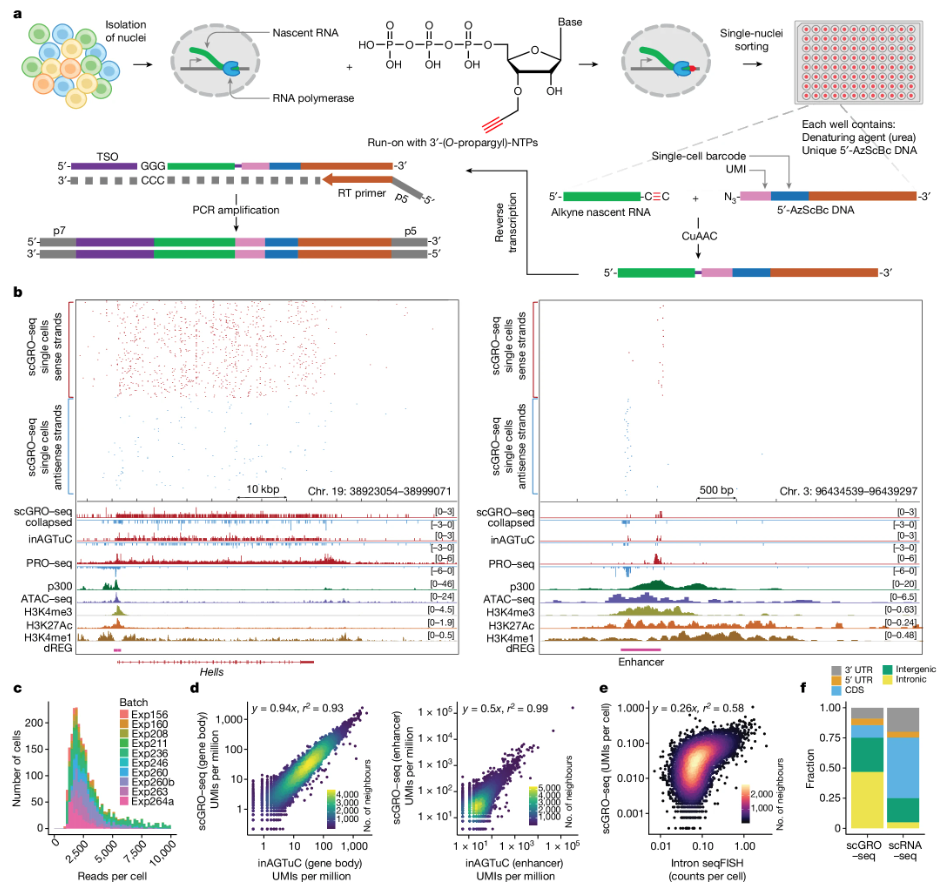
首先,作者開(kāi)發(fā)了一種利用點(diǎn)擊化學(xué)(AGTuC)的全基因組轉(zhuǎn)錄組測(cè)序方法,是一種基于細(xì)胞群的新生RNA測(cè)序方法,通過(guò)3′-(O-propargyl)-NTPs選擇性標(biāo)記新生RNA,偶聯(lián)5′端帶有AzScBc基團(tuán)的DNA PCR handle,逆轉(zhuǎn)錄RNA-DNA偶聯(lián)物并制備N(xiāo)GS文庫(kù)。為了能夠?qū)⒃摲椒ǜ玫膽?yīng)用于單細(xì)胞測(cè)序,作者進(jìn)一步優(yōu)化AGTuC實(shí)驗(yàn)條件,在標(biāo)記過(guò)程中不會(huì)破壞核膜完整性,稱(chēng)為完整核AGTuC(inAGTuC)。作者利用inAGTuC測(cè)試了不同細(xì)胞核投入量下捕獲新生RNA的效率并與PRO-seq進(jìn)行相關(guān)性比較,結(jié)果發(fā)現(xiàn) AGTuC 和 inAGTuC具有更高的效率、更低的成本、更短的文庫(kù)制備時(shí)間和更低的樣品起始量,是現(xiàn)有方法(PRO-seq)的可行替代方案,同時(shí)為單細(xì)胞新生 RNA 測(cè)序奠定了基礎(chǔ)。
在inAGTuC的基礎(chǔ)上,作者開(kāi)發(fā)了新的化學(xué)物質(zhì)應(yīng)用于單細(xì)胞新生RNA測(cè)序,將其命名為scGRO-seq。首先分離細(xì)胞核,加入3′-(O-propargyl)-nucleotides進(jìn)行核run-on反應(yīng),將附有3′標(biāo)記的新生RNA完整細(xì)胞核通過(guò)流式分選至含有尿素的96孔板中(尿素可以裂解核膜并使 RNA 聚合酶變性并釋放標(biāo)記的新生 RNA),將帶有5′-AzScBc基團(tuán)的DNA接頭(包括位于5'-AzScBc 、10-12bp單細(xì)胞barcode序列、4-6bp UMI序列和 PCR handle)和CuAAC MIX加入孔板中,在CuAAC的作用下,炔丙基標(biāo)記的新生RNA與每個(gè)孔中唯一的5′-AzScBc DNA連接形成RNA-DNA偶聯(lián)物,將孔板中RNA合并,加入TSO序列通過(guò)M-MuLV逆轉(zhuǎn)錄酶進(jìn)行反轉(zhuǎn)錄,結(jié)束后通過(guò)Cas9去除空接頭,最后進(jìn)行擴(kuò)增和測(cè)序。
scGRO-seq直接測(cè)定轉(zhuǎn)錄爆發(fā)動(dòng)力學(xué)
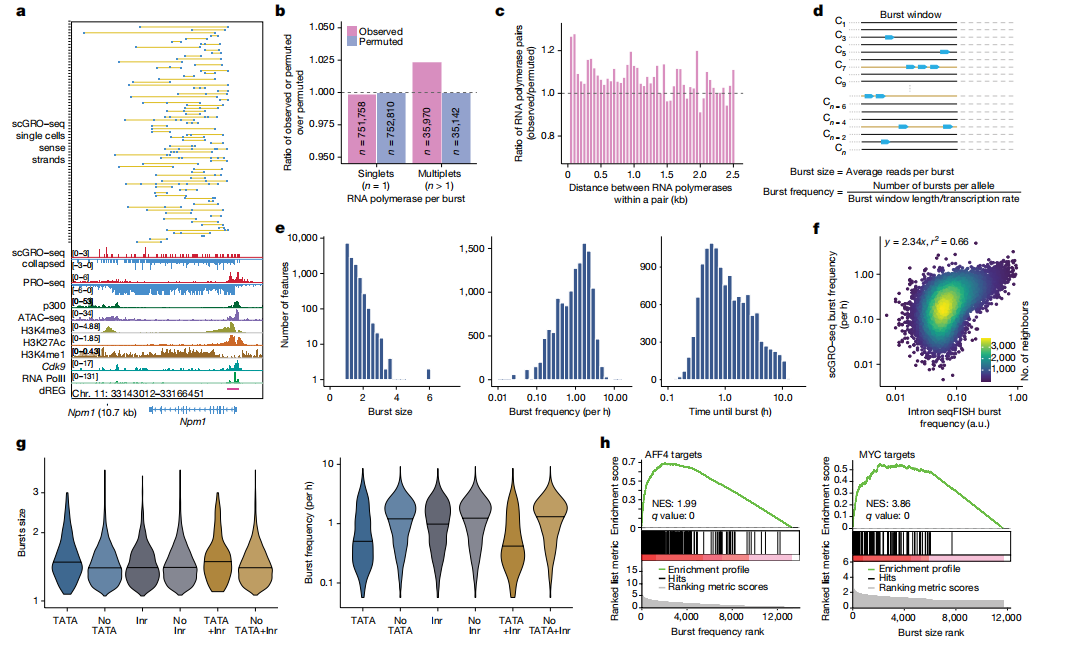
與傳統(tǒng)熒光原位雜交檢測(cè)轉(zhuǎn)錄動(dòng)力學(xué)的方法不同,scGRO-seq能夠以單核苷酸分辨率檢測(cè)全基因組正在轉(zhuǎn)錄的RNA聚合酶,能夠觀察到RNA聚合酶在基因上的分布,反映了轉(zhuǎn)錄的動(dòng)態(tài)過(guò)程(圖2a)。為了驗(yàn)證scGRO-seq能夠揭示轉(zhuǎn)錄爆發(fā)的過(guò)程,作者設(shè)計(jì)了一個(gè)無(wú)偏倚的模型,量化轉(zhuǎn)錄RNA聚合酶的發(fā)生頻率,結(jié)果發(fā)現(xiàn),在真實(shí)數(shù)據(jù)中出現(xiàn)更高的多聚體,表示多個(gè)RNA聚合酶同時(shí)轉(zhuǎn)錄(圖2b),同時(shí)分析了多聚體之間的距離分布發(fā)現(xiàn),真實(shí)數(shù)據(jù)中多聚體具有更緊密的RNA聚合酶分布(圖2c),進(jìn)一步說(shuō)明了scGRO-seq能夠捕獲到轉(zhuǎn)錄爆發(fā)現(xiàn)象。作者通過(guò)scGRO-seq數(shù)據(jù)直接測(cè)定了轉(zhuǎn)錄爆發(fā)的動(dòng)力學(xué)參數(shù)(圖2d-e),比較發(fā)現(xiàn)scGRO-seq與內(nèi)含子 seqFISH所得爆發(fā)頻率數(shù)據(jù)具有良好相關(guān)性(圖2f),同時(shí)發(fā)現(xiàn)核心啟動(dòng)子元件和轉(zhuǎn)錄因子可以調(diào)節(jié)轉(zhuǎn)錄爆發(fā)參數(shù)(圖2g-h)。
綜上所述,scGRO-seq能夠直接和全面地觀察轉(zhuǎn)錄爆發(fā),有助于在單細(xì)胞水平上研究轉(zhuǎn)錄動(dòng)力學(xué)。
圖2 scGRO-seq推斷轉(zhuǎn)錄動(dòng)力學(xué)
scGRO-seq推斷組蛋白基因的細(xì)胞周期
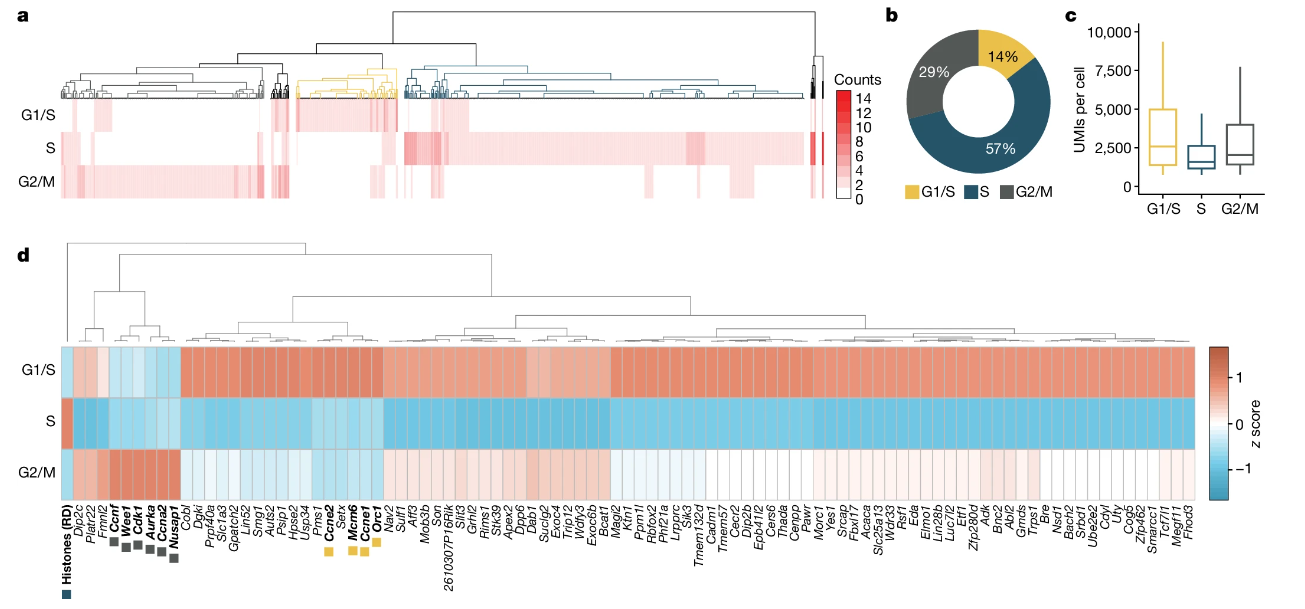
目前,用于確定的細(xì)胞周期狀態(tài)的傳統(tǒng)scRNA-seq方法存在一定局限性,首先是大多數(shù)scRNA-seq依賴(lài)于poly(A)尾進(jìn)行捕獲測(cè)序,因此無(wú)法檢測(cè)到復(fù)制依賴(lài)性組蛋白基因(在S期專(zhuān)門(mén)轉(zhuǎn)錄的最佳細(xì)胞周期期特異性基因,無(wú)poly(A)尾);其次,這些基因高度特異表達(dá)于S期,在前期樣本制備時(shí)可能存在一定滯后性,最終導(dǎo)致難以及時(shí)檢測(cè)到特異性基因表達(dá)。而scGRO-seq能夠解決傳統(tǒng)scRNA-seq存在的問(wèn)題,作者利用scGRO-seq對(duì)小鼠胚胎干細(xì)胞進(jìn)行實(shí)驗(yàn),結(jié)果發(fā)現(xiàn),scGRO-seq檢測(cè)到組蛋白位點(diǎn)體中復(fù)制依賴(lài)性組蛋白基因的活性轉(zhuǎn)錄,并且可對(duì)S 期細(xì)胞進(jìn)行分類(lèi)(圖3a),通過(guò)不同細(xì)胞周期期特異性基因表達(dá)的分層聚類(lèi)揭示單個(gè)細(xì)胞的三個(gè)重要簇,三個(gè)簇具有不同的細(xì)胞比例代表細(xì)胞不同周期階段的長(zhǎng)度(圖3b),不同細(xì)胞周期轉(zhuǎn)錄水平存在差異(圖3c)。對(duì)細(xì)胞周期階段差異表達(dá)基因的分析發(fā)現(xiàn),細(xì)胞在DNA復(fù)制過(guò)程中雖然轉(zhuǎn)錄水平降低,但會(huì)持續(xù)進(jìn)行,不同基因存在不同轉(zhuǎn)錄循環(huán)模式(圖3d)。
綜上所述,scGRO-seq能夠揭示整個(gè)細(xì)胞周期的動(dòng)態(tài)轉(zhuǎn)錄程序。
圖3 scGRO-seq推斷組蛋白基因的細(xì)胞周期
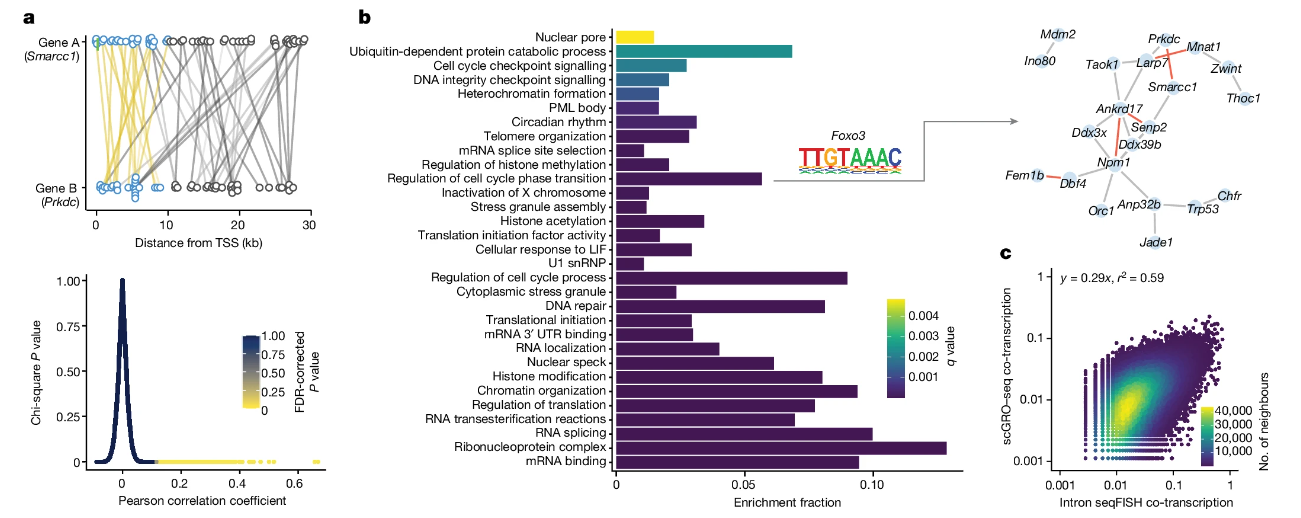
作者利用scGRO-seq探究功能相關(guān)基因是否在穩(wěn)態(tài)下進(jìn)行共轉(zhuǎn)錄。通過(guò)可視化方法直觀地展示了兩個(gè)基因在單細(xì)胞水平上的共轉(zhuǎn)錄關(guān)系,表明這兩個(gè)基因可能在時(shí)間上或功能上有某種聯(lián)系,比如可能受到相同的轉(zhuǎn)錄因子調(diào)控,或者參與相同的生物學(xué)過(guò)程(圖4a)。作者對(duì)轉(zhuǎn)錄過(guò)程中共表達(dá)的基因?qū)M(jìn)行分析發(fā)現(xiàn)了共轉(zhuǎn)錄基因?qū)υ诩?xì)胞周期調(diào)控、RNA剪接、翻譯控制等生物學(xué)過(guò)程中富集(圖4b)。作者將scGRO-seq獲得的共轉(zhuǎn)錄基因?qū)εc內(nèi)含子seqFISH比較共轉(zhuǎn)錄相關(guān)性,結(jié)果發(fā)現(xiàn)兩者具有高度相似的共轉(zhuǎn)錄譜(圖4c)。
綜上所述,具有高通量?jī)?yōu)勢(shì)的scGRO-seq能夠直接檢測(cè)基因?qū)蚧蚓W(wǎng)絡(luò)之間的轉(zhuǎn)錄協(xié)調(diào)性,是研究基因組功能的重要工具。
圖4 功能相關(guān)基因的協(xié)調(diào)轉(zhuǎn)錄
增強(qiáng)子-基因時(shí)間協(xié)調(diào)
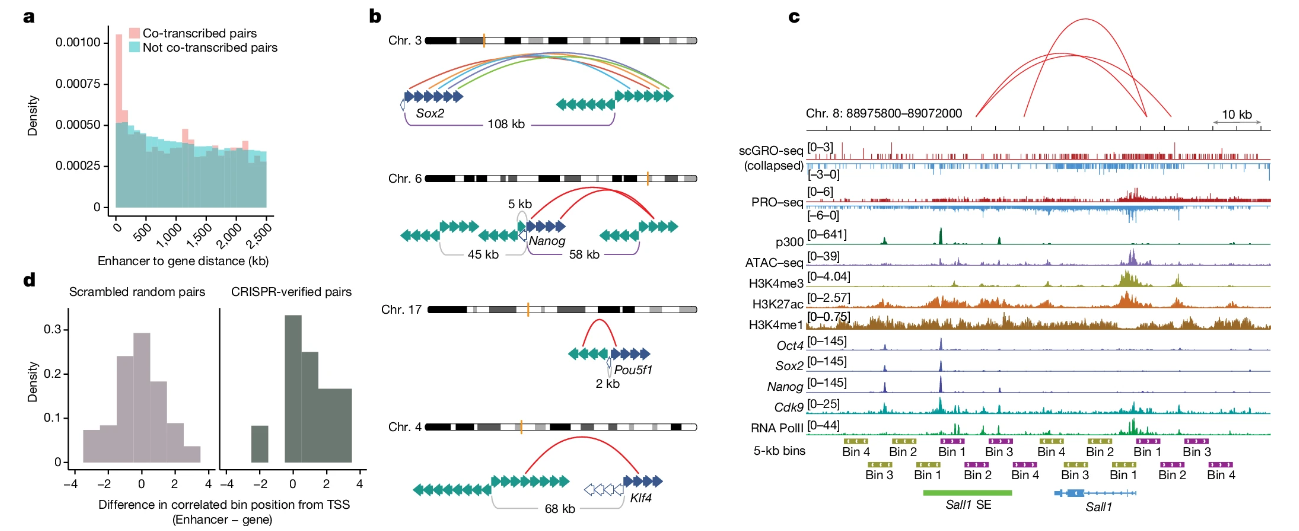
作者利用scGRO-seq探究基因和增強(qiáng)子之間的時(shí)間協(xié)調(diào)性。作者分析了基因前 10 kb 內(nèi)的 scGRO-seq讀段以及增強(qiáng)子周?chē)蛲廪D(zhuǎn)錄的每條鏈上至少 3 kb 的讀段,結(jié)果發(fā)現(xiàn)增強(qiáng)子-基因共轉(zhuǎn)錄主要在 200 kb 內(nèi)顯著富集(圖5a),同一條染色體上的功能相關(guān)基因聚集在一起時(shí),多個(gè)增強(qiáng)子與每個(gè)基因相關(guān),可能是細(xì)胞周期調(diào)控的進(jìn)一步作用所導(dǎo)致結(jié)果(圖5b)。為了驗(yàn)證增強(qiáng)子的轉(zhuǎn)錄可能在其靶基因啟動(dòng)子轉(zhuǎn)錄之前開(kāi)始的假設(shè),作者通過(guò)CRISPR干擾驗(yàn)證多個(gè)增強(qiáng)子bin與該基因之間存在相關(guān)性(圖5c),同時(shí)發(fā)現(xiàn)相關(guān)的增強(qiáng)子bin通常比基因bin距離其 TSS 更遠(yuǎn),這意味著增強(qiáng)子轉(zhuǎn)錄可能在啟動(dòng)子轉(zhuǎn)錄之前開(kāi)始(圖5d)。
綜上所述,scGRO-seq初步驗(yàn)證了增強(qiáng)子轉(zhuǎn)錄可能在啟動(dòng)子轉(zhuǎn)錄之前開(kāi)始,但該時(shí)間模式對(duì)增強(qiáng)子-基因轉(zhuǎn)錄調(diào)控的影響需進(jìn)一步深入探究。
圖5 基因與增強(qiáng)子之間的時(shí)間協(xié)調(diào)
綜上所述,scGRO-seq可以不依賴(lài)于Poly(A)尾檢測(cè)新生RNA,通過(guò)CuAAC可以捕獲約10%的新生RNA,作者通過(guò)點(diǎn)擊化學(xué)取代了多輪新生的RNA純化和核酸連接,優(yōu)化了實(shí)驗(yàn)步驟,增加高通量液滴封裝捕獲效率,擴(kuò)展了scGRO-seq的適用性。
scGRO-seq本質(zhì)上是多模態(tài)的,是一個(gè)可以深入詳細(xì)地理解轉(zhuǎn)錄調(diào)控的工具,它可以在天然環(huán)境中評(píng)估共轉(zhuǎn)錄和預(yù)測(cè)增強(qiáng)子-基因調(diào)控網(wǎng)絡(luò),文中作者已驗(yàn)證scGRO-seq可以確定表達(dá)基因的突發(fā)大小和頻率、細(xì)胞周期階段的轉(zhuǎn)錄動(dòng)力學(xué)以及全基因組基因-基因和增強(qiáng)子-基因共轉(zhuǎn)錄檢測(cè)等功能。
但目前的scGRO-seq仍具有一定局限性。通過(guò)低sarkosyl濃度實(shí)現(xiàn)的核完整性的保持未能促進(jìn)暫停復(fù)合物中RNA聚合酶的運(yùn)行,從而限制了啟動(dòng)子-近端暫停聚合酶的檢測(cè)。在讀取深度和細(xì)胞數(shù)量方面限制了對(duì)基因-基因和增強(qiáng)子-基因?qū)Φ谋l(fā)動(dòng)力學(xué)和共轉(zhuǎn)錄的分析。但盡管存在這些局限性,scGRO-seq的適應(yīng)性和效率為研究不同生物學(xué)背景下的轉(zhuǎn)錄動(dòng)力學(xué)和調(diào)控機(jī)制提供了新的途徑,豐富了對(duì)基因表達(dá)調(diào)控及其在生理和病理?xiàng)l件下的影響的理解。