
2024-07-09

在當今飛速發展的醫療健康領域,醫學前沿的探索與臨床實踐的革新正以前所未有的速度推進,深刻影響著人類疾病的預防、診斷、治療及康復過程。隨著高通量測序、質譜檢測、生物信息學、人工智能、精準醫療等高新技術的不斷融合與應用,臨床醫學正經歷著一場前所未有的變革。從癌癥的個性化治療到罕見病的基因療法,從基于大數據的疾病預測模型到遠程醫療技術的普及,每一項進步都在拓展醫療服務的邊界,提升醫療質量與效率。
然而,醫學知識的爆炸性增長也帶來了挑戰。因此,匯總當前醫學前沿的研究進展與臨床熱點,不僅對促進學術交流、加快科研成果轉化至關重要,也是滿足健康需求、提升健康素養的重要途徑。總覽當前研究熱點與挑戰,了解未來研究的重點領域和潛在突破口,促進醫學科學的持續創新和發展。
專題一 微生物組與健康的關系
微生物從人類誕生之日起便與之進行共同進化,形成了復雜的互作關系。其中,微生物的移位或其產生的代謝物通過擾動人體免疫系統,從而影響與其他器官相關的功能,最終形成了這種有趣的互作模式類似“軸“的關系。微生物-器官軸多組學分析可以全面覆蓋各賽道臨床疾病,且其應用中正處于發展階段,其中新的技術研究方法不僅可以進一步提高臨床醫生及基礎醫學研究學者對疾病生物學的認識,在不久的將來將極大地推動臨床疾病的個性化精準治療。
腸道菌群-器官軸是指定植在腸道的微生物菌群與其它部位器官(腦、腎臟、肝臟、皮膚等)進行雙向或多向交流的系統(圖1)。在這個軸系統中,腸道菌群通過分泌小分子、酶、毒素等代謝物對宿主的代謝和生理過程進行調控,從而影響機體的健康狀態和疾病發展。近年來,國家自然科學基金委設立了多項關于人體微生物組研究的重大課題與重點項目,聚焦于人體微生態系統的結構解析、功能挖掘以及與健康和疾病關聯性的基礎研究。
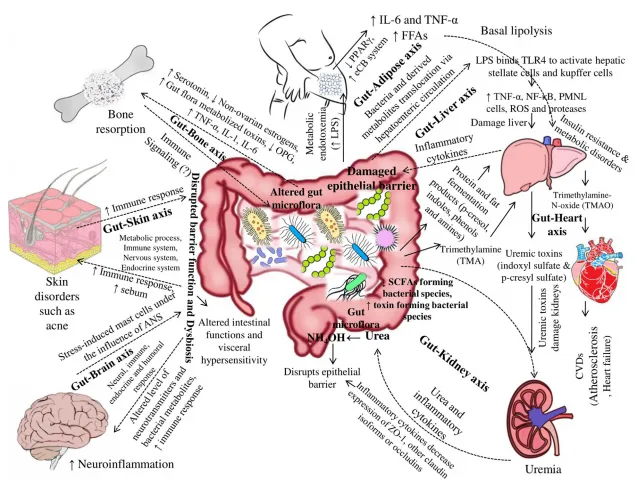
圖1 腸道菌群-器官軸示意圖
微生物-器官軸的研究方向主要是為了回答微生物介導疾病的生物學機制。例如解決肝炎-肝硬化-肝癌的發生的科學問題,我們可以利用腸道微生物-肝器官軸,結合宏基因組、人體代謝組、單細胞轉錄組、代謝組等技術從各個維度和角度來提供科學證據,從而更加全面地、深入地回答相應的科學問題。
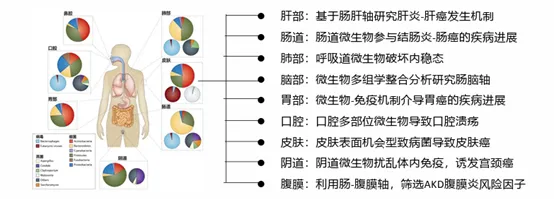
圖2 微生物-器官軸研究方向
專題二 微生物-器官軸分類
2.1、微生物-腸道軸(點擊閱讀詳情)
微生物-腸道軸(Microbiota-Gut Axis):最為人熟知的微生物-器官軸,腸道微生物與腸道上皮細胞、免疫細胞緊密互動,影響營養吸收、能量代謝、免疫系統發育及功能、以及神經信號傳遞(通過腸-腦軸)。
2.2、微生物-肝臟軸(點擊閱讀詳情)
微生物-肝臟軸(Microbiota-Liver Axis):腸道微生物通過門靜脈系統與肝臟直接相連,影響肝臟的代謝、解毒功能及炎癥狀態。失衡的腸道菌群可導致脂肪肝、肝炎乃至肝硬化等疾病。
2.3、微生物-肺軸(點擊閱讀詳情)
微生物-肺軸(Microbiota-Lung Axis):盡管肺部傳統上被認為是無菌環境,但越來越多證據表明,呼吸道微生物與肺部疾病(如哮喘、慢性阻塞性肺病)有關聯,通過氣溶膠傳播或微生物移位影響肺部健康。
2.4、微生物-腦軸(點擊閱讀詳情)
微生物-腦軸(Microbiota-Brain Axis):包括腸-腦軸,指腸道微生物通過神經、內分泌及免疫途徑與大腦溝通,影響情緒、認知功能、應激反應及睡眠等。微生物產生的代謝產物能穿越血腦屏障,影響神經遞質平衡。
2.5、微生物-皮膚軸(點擊閱讀詳情)
微生物-皮膚軸(Microbiota-Skin Axis):皮膚上的微生物群落參與局部免疫調節,對抗病原體入侵,影響皮膚健康與疾病,如濕疹、銀屑病等皮膚病。
2.6、微生物-口腔(點擊閱讀詳情)
口腔菌群是人體微生物組重要組成部分,具有高度的多樣性,包括數百種細菌、真菌、古菌和病毒等。不同的口腔部位如舌苔、口腔粘膜、牙菌斑具有獨特的微生物物種組成,共同形成了復雜的生態系統。俗話說“病從口入”,口腔菌群在很多疾病的發生過程扮演重要的角色。
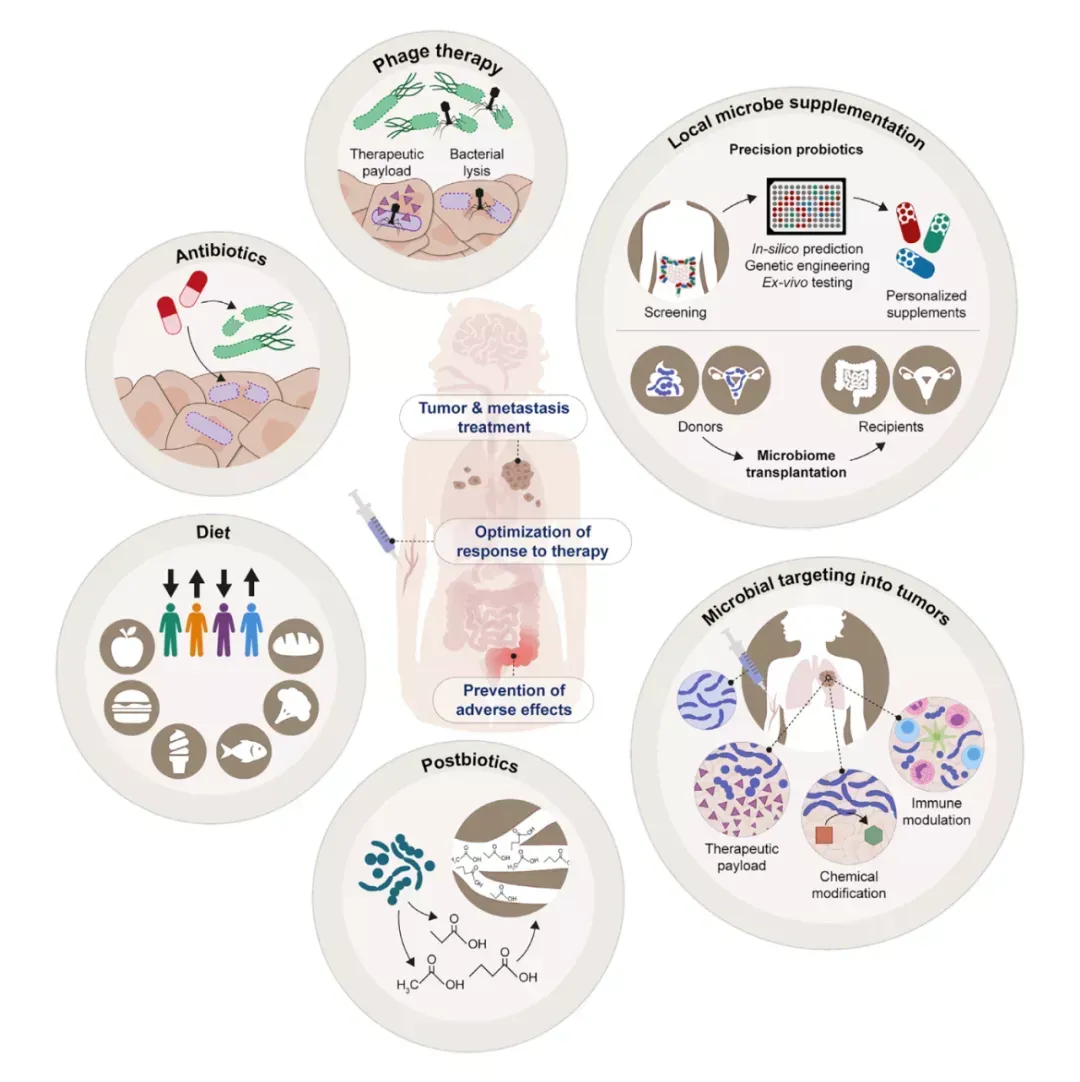
圖3 器官軸分類
專題三 微生物-腫瘤發展與癌癥治療
微生物組與癌癥之間存在密切關系,這種關系正在成為醫學研究領域的一個新興焦點。微生物組與癌癥的關系可以從三方面去認識:
(1)某些已知的微生物病原體能直接導致癌癥的發生,這些微生物也被稱為致癌物,比如HPV病毒與宮頸癌、幽門螺桿菌與胃癌、EBV病毒與鼻咽癌等;
(2)人體共生微生物與癌癥發生的協同關系,研究表明腸道菌群或口腔菌群的失調能通過微生物-器官軸影響遠端器官腫瘤的發生發展;
(3)腫瘤內生微生物與癌癥的關系,腫瘤組織內微生物通過調節腫瘤微環境促進或抑制腫瘤的發展。
微生物組與癌癥存在復雜的互作關系,既有正面的抗癌作用,也有反面的致癌作用。深入研究這種關系,有助于我們更好地理解癌癥的發生機制,開發新的預防和治療方法,為癌癥患者帶來更多的希望和可能。
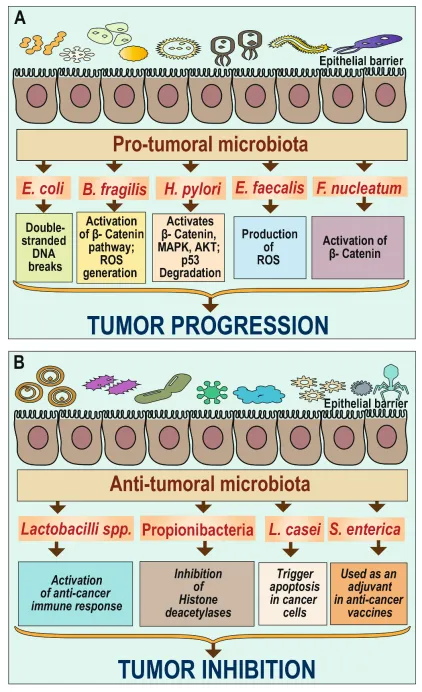
圖4 微生物組與腫瘤的互作關
專題四 微生物組-器官軸研究思路

文章題目:The microbial metabolite trimethylamine N-oxide promotes antitumor immunity in triple-negative breast cancer
期刊:Cell Metabolism(IF:27.7)
技術手段:16S rRNA基因V3V4區測序、代謝組
乳腺癌的發病率逐年增高,并成為中國女性發病率最高的惡性腫瘤,是名副其實的“紅顏殺手”。其中,三陰性乳腺癌(TNBC)惡性程度較高,患者生存預后較差,易出現早期復發和轉移,且既往缺乏有效的針對性治療策略,素有最“毒”乳腺癌之稱。
與常見研究中報道的抗腫瘤激活劑直接作用于免疫細胞發揮功效不同,該文從獨特視角出發,發現特殊微生物群落借助代謝產物氧化三甲胺(Trimethylamine N-oxide,TMAO),能夠直接作用于腫瘤細胞,誘導其焦亡,繼而促進免疫細胞浸潤,最終發揮抗腫瘤作用。

文章題目:Hyodeoxycholic acid alleviates non-alcoholic fatty liver disease through modulating the gut-liver axis
期刊:Cell Metabolism(IF:27.7)
技術手段:轉錄組、宏基因組、膽汁酸靶向代謝組
非酒精性脂肪性肝病(NAFLD)被認為是一種影響全球約四分之一人口的流行病。但驅動NAFLD發生和發展的病因和病理因素尚未完全闡明。此外,尚未有抗NAFLD藥物得到國際權威機構的批準。膽汁酸(BAs)是一組由肝細胞內膽固醇合成的兩親性分子,BA-腸道菌群串擾與包括NAFLD在內的代謝性疾病有關,在調節宿主葡萄糖和脂質代謝中起重要作用。前期研究顯示非12α-羥基化膽汁酸、豬膽酸(HCA)和豬脫氧膽酸(HDCA)在調節葡萄糖穩態和預測2型糖尿病未來風險方面具有治療潛力。因此假設了一種藥物治療策略,通過靶向替代BA合成通路來治療代謝性疾病。